精准前沿丨基于Olink平台的泛癌血液蛋白组学分析肿瘤特征蛋白和早筛模探索
本期《精准前沿》栏目分享来自瑞典皇家理工学院研究团队发表于Nature Communications(IF=16.6)上的一篇研究[1],该研究使用一种新的肿瘤研究技术平台——Olink Explore血液检测蛋白技术和泛癌分析策略,通过对主要癌症类型的患者血液的蛋白质水平进行全面分析,探索不同癌种的蛋白质组特征,并构建能够准确预测癌种的分类器模型以及肿瘤早筛预测模型。

研究背景
肿瘤防治最重要且最有效的方式是通过及早发现避免肿瘤的进展、转移和出现难治性肿瘤,从而改善患者的预后生存。而在过去的十年里,利用基因组学开展的研究并未实现治疗方案的实质性改变,也未促进大规模人群癌症筛查的开展,仍缺乏针对不同类型癌症筛查的有效方法。
最新研究表明,肿瘤患者的血液蛋白质组谱有助于更好地了解肿瘤的发生进展,从而实现更早地明确诊断、进行患者的风险预测和癌症分型。而下一代血液蛋白检测技术基于抗体的PEA与NGS测序相结合,用于量化多种血液蛋白质浓度,为低成本的泛癌症人群筛查提供了可能。
研究设计
研究团队使用 Olink Explore 1536 panel 平台对来自12种癌症的1477名患者:Top 5 癌种为肺癌 (n=268)、结直肠癌 (n=221)、神经胶质瘤 (n=145)、前列腺癌癌症(n=163)和乳腺癌 (n=152) ,以及74名健康个体的血浆蛋白质组进行了检测。Olink Explore平台仅需要不到3μL的血浆即可对1463种蛋白质进行相对定量。
文章主要设计思路如图1所示。研究团队通过差异分析以及根据机器学习预测建模的权重排序为每个癌种选择了一组特征蛋白,并基于所选特征蛋白合集构建多分类模型,精确区分患者的肿瘤类型。并根据特征蛋白Panel建立肿瘤预测模型,对健康队列中的每种癌症进行分类,进一步验证了所选生物标志物潜力,并最终证实这种分类可以准确识别早期癌症患者。
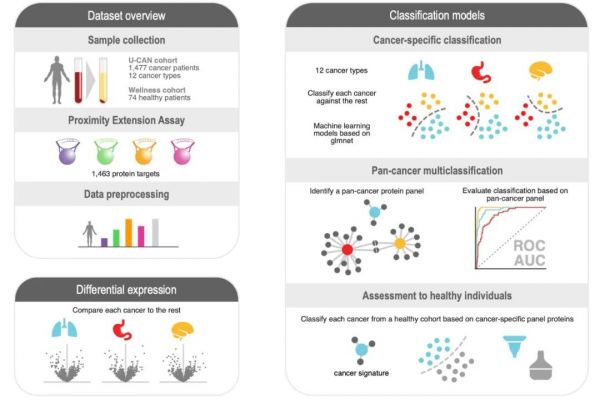
图1. 研究设计
研究结果
1.不同癌种的特征蛋白
研究者通过双边T检验结合Benjamini-Hochberg多重假设矫正,校正后P值的显著性阈值为0.05,评估了目标癌种与其他癌种的显著差异表达蛋白(图2A)。在图 2b 中,显示了 12 种癌症中上调和下调的蛋白质数量。结果表明,大部分panel内设计的蛋白质都存在差异表达。而不同癌种的差异表达蛋白也反映了其癌种的特征,例如免疫细胞相关癌症(AML、CLL 和淋巴瘤)中的上调蛋白大部分与免疫调节相关。
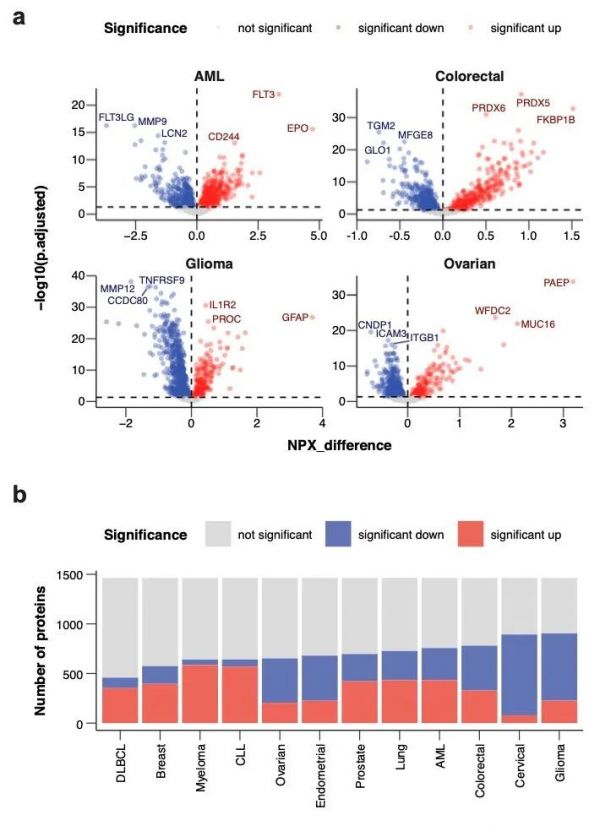
图2. 各个癌种的差异蛋白分析
2. 癌种单分类器模型
研究团队为每种癌症类型(n=12)构建了基于AI的疾病预测模型:分别使用所有定量的蛋白质(n=1463)和70%的癌症患者作为训练集,选择基于正则化广义线性模型的机器学习算法“glmnet”, 在测试集上的验证结果如图3a所示,展示了每个癌种队列分类正确的概率,图3b反映了每个癌种预测的AUC面积在0.8-1之间,其中三个与免疫细胞相关的癌症:AML、CLL 和骨髓瘤,观察到特别高的置信度,它们的 AUC 均为 0.99-1。
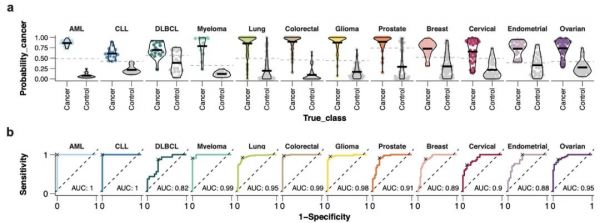
图3. 癌种分类器模型
3. 癌种多分类器模型
基于上述结果,研究团队根据 glmnet 模型的权重排名以及显著差异分析结果,构建了一组包括83个蛋白的多分类器预测模型panel(图4),使用以下纳入标准: (i) 癌症分类模型表明总体重要性超过 50% 的蛋白质; (ii) 差异表达分析确定为上调的蛋白质;
(iii) 每种癌症至少有 3 个蛋白质。
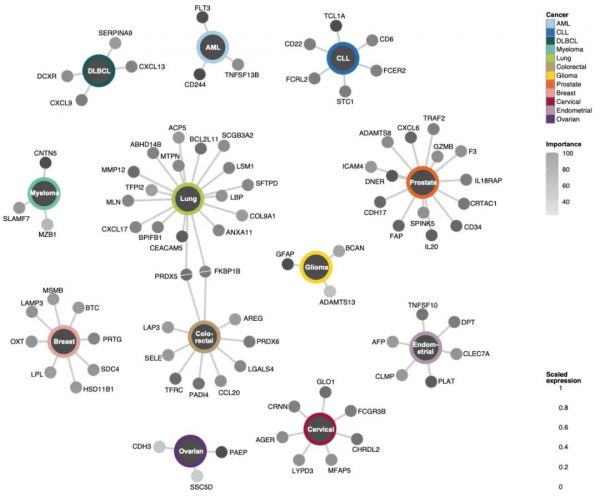
图4. 83 panel 癌种多分类器蛋白
作者根据不同的蛋白质选择方式,构建了四种不同的分类模型进行性能比较:(i) 所有蛋白质 (n = 1463);(ii) 83panel中选择的蛋白质(iii)每种癌症的三种最重要的蛋白质(n = 36)和(iv)每种癌症的单一最重要的蛋白质(n = 12);结果显示,使用蛋白质组(n = 83)的预测性能与使用全部蛋白的性能相当,显著优于仅使用每种癌症最显著的蛋白质标记物(图5)。这也证明了使用血浆蛋白质组的额外优势,例如乳腺癌患者的单个标记物没有选择性,但使用多种蛋白质的预测模型产生了更准确的分型。
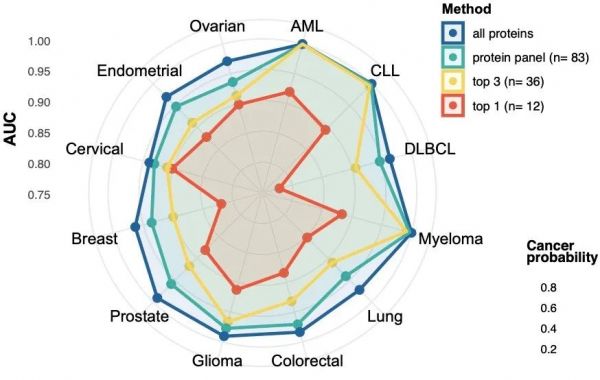
图5. 多分类器模型评估
4. 肿瘤早筛早诊预测
研究团队进一步分析了健康人和肿瘤患者之间的差异蛋白,并重点关注了人群基数较大以及样本量较多的结直肠癌和肺癌患者。结果显示,基于不同癌种的特征蛋白,不仅可以区分不同癌种,也能够很准确的区分癌症患者和健康对照(AUC均高于0.83,图6a-d)。而一些特征蛋白的表达在癌种的不同疾病分期也存在显著性差异,例如用于识别CLL患者的CD22和结直肠癌患者中的LGALS4(图6e)。在样本较多的肺癌和结直肠癌上,观察到血浆蛋白质组区分I期肺癌患者和健康个体的AUC为0.79;区分I期结直肠癌患者和健康对照的AUC为0.78,早期和晚期癌症患者的模型表现没有显着差异(图6 f-g)。
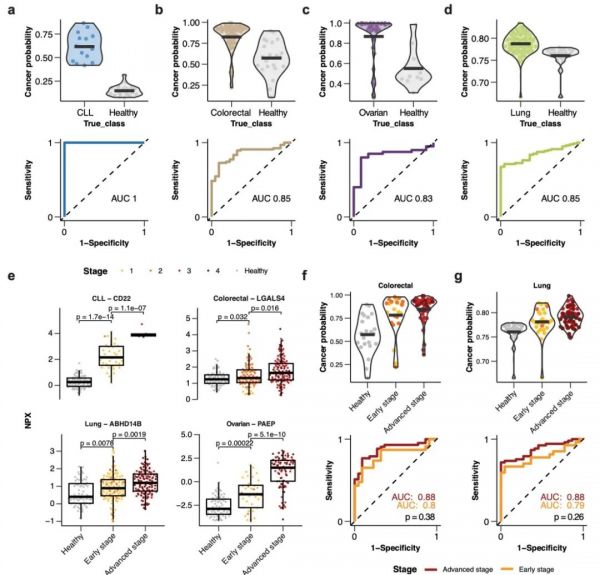
图6. 肿瘤早筛早诊预测
讨论
研究团队基于Olink平台通过比较不同类型癌症患者的血浆蛋白组图谱,找到每种类型癌症的特异性标记,构建预测模型用以区分不同癌症类型,并且该模型还能够检测肿瘤早期患者。作者也指出,该模型的应用还需要更多的独立验证集的预测性能评估以及跨平台蛋白组学一致性的评估,但为大人群样本的广泛早筛提供了新的思路。除此之外,作者还开放了该研究中12种不同癌症类型的1400多名癌症患者的蛋白组学数据供其他研究者参考使用。
Olink新一代蛋白组学平台可实现高通量、高特异性、高灵敏度、高动态范围的靶向蛋白质组定量检测,已在基础科研、医药研发及临床试验中研究得到广泛认可和应用。先声诊断旗下专注于CRO业务品牌新标智钥(Simarker),在国内首批引进了Olink™ Signature Q100平台,正式开展高敏蛋白组学检测和分析服务。
目前,先声诊断在蛋白类生物标志物检测平台覆盖了Simoa、Olink、MSD和ELISA等不同通量、不同技术灵敏度、不同线性范围的检测平台,可为蛋白类生物标志物的开发和研究提供完善的解决方案。
END
参考文献: [1] Uhlén M. Next generation pan-cancer blood proteome profiling using proximity extension assay. Nat Commun. 2023 Jul 18;14(1):4308. doi: 10.1038/s41467-023-39765-y. PMID: 37463882; PMCID: PMC10354027.
撰写丨阿晖 编辑、排版丨SX
本文由“健康号”用户上传、授权发布,以上内容(含文字、图片、视频)不代表健康界立场。“健康号”系信息发布平台,仅提供信息存储服务,如有转载、侵权等任何问题,请联系健康界(jkh@hmkx.cn)处理。
相关知识
AI如何助力重塑肿瘤诊疗模式
《自然》子刊:华科刘刚团队发现,8种健康膳食模式的蛋白组学特征谱与糖尿病、心血管病等慢性代谢性疾病
全肿瘤的遗传因素:基因如何影响肿瘤发展
瘦型非酒精性脂肪肝的临床特征和蛋白质组学分析,Frontiers in Endocrinology
院士卢煜明:血浆DNA片段学在液体活检的应用将助力精准医学领域实现更多突破
关于孕妇蛋白尿的基本信息介绍
《中国恶性肿瘤学科发展报告(2021)》—肿瘤营养未来展望篇
预测上百种疾病风险,发现26个潜力新靶点!《细胞》:复旦团队绘制人类健康与疾病蛋白质组图谱
一次平扫CT 筛查多种癌症(大健康观察)
缺少蛋白质会导致脸水肿吗
网址: 精准前沿丨基于Olink平台的泛癌血液蛋白组学分析肿瘤特征蛋白和早筛模探索 https://www.trfsz.com/newsview213164.html
推荐资讯
- 1从出汗看健康 出汗透露你的健 3963
- 2早上怎么喝水最健康? 3743
- 3习惯造就健康 影响健康的习惯 3379
- 4五大原因危害女性健康 如何保 3282
- 5连花清瘟、布洛芬等多款感冒药 3006
- 6补肾吃什么 补肾最佳食物推荐 2517
- 7男子喝水喉咙里像放了刀子一样 2510
- 810人混检核酸几天出结果?1 2267
- 9第二轮新冠疫情要来了?疾控中 2260
- 10转阴多久没有传染性?满足四个 2207






