Cell, Science 特刊——聚焦生命早期免疫系统发展的调控因素和作用机制
免疫系统 (immune system) 是防卫病原体入侵最有效的武器。
面对神秘且强大的免疫系统,我们还有很多的疑问 —— 生命的早期,免疫系统是如何逐渐形成的呢?免疫系统的形成受到哪些因素的调控?疫苗如何接种可以更好地保护婴儿?
近年来,研究者对胎儿 - 新生儿免疫系统的复杂性和发展轨迹有了更好的了解,进而我们意识到,生命早期的免疫系统并不是孤立发展的,而是受到母体细胞、共生微生物和病原体的强烈影响。

图片来源:站酷海洛 Plus
在新生儿阶段,母亲用母乳来喂养新生婴儿,通过母乳来转移粘膜和全身免疫的记忆。Cell、Science 特刊发表多篇文章,聚焦胎儿 - 新生儿免疫系统,总结了生命早期免疫系统发展的调控因素和作用机制等。
研究内容:
非遗传的、非表观遗传的、非微生物的免疫调节「肠 - 乳腺轴」
调节性 T 细胞(Tregs)能够有效抑制自身反应性免疫反应,避免免疫系统对自身的组织器官进行攻击,而调节性 T 细胞功能丧失后会导致致命的自身免疫性疾病。调节性 T 细胞根据是否表达两个转录因子,可以进一步被细化为两个亚类,即 Helios+Tregs 和 RORγ+Tregs。在哺乳期小鼠是否产生 RORγ+Treg,是其抵御肠炎和结肠癌的关键因素。
5 月 12 日在 Cell 杂志上发表的来自美国哈佛医学院 Christophe Benoist 和 Diane Mathis 研究组题为 An Immunologic Mode of Multigenerational Transmission Governs a Gut Treg Setpoint 的论文中,研究者发现了一种非遗传的、非表观遗传的、非微生物的母胎 RORγ+Treg 传递模式,并提出了「肠 - 乳腺轴」(entero-mammary axis)的概念。
研究者将遗传背景不同的新生小鼠在一定的窗口期内交给同一只母鼠喂养后,它们肠道的 RORγ+Treg 水平与母鼠类似,并终生稳定。此外,小鼠肠道的 RORγ+Treg 比例与免疫球蛋白 IgA 的产生、血清与乳汁 IgA 水平和肠膜的 IgA 包被程度呈负相关,这种性状也由母体传播。
这种免疫学传递模式可以提供适应性,并调节免疫反应和肠道炎症性疾病易感性相关的基因。
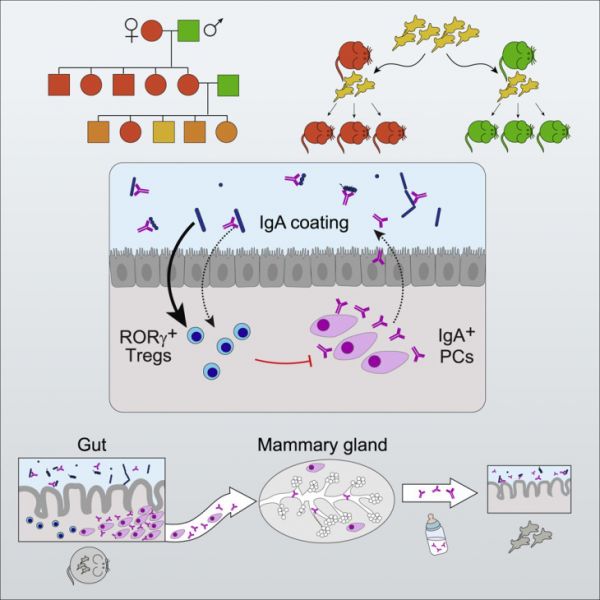 图 1 图片来源:Cell 生命早期免疫系统发展的调控因素和作用机制
图 1 图片来源:Cell 生命早期免疫系统发展的调控因素和作用机制2020 年 5 月 8 日,Science 推出了一期名为 Early life immunology——The immune system's first steps 的特刊。这期特刊中包括了四篇综述,综述了早期生命免疫学领域的最新进展,总结了生命早期免疫系统发展的调控因素和作用机制。
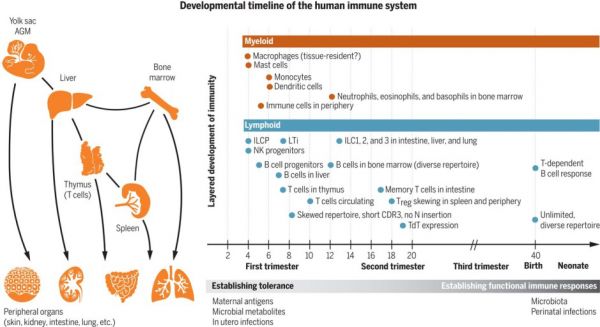
 图 2 Science 特刊图片来源:Science胎儿免疫系统发育规律
图 2 Science 特刊图片来源:Science胎儿免疫系统发育规律第一篇综述来自英国 Wellcome Sanger 研究所的研究人员 Jong-Eun Park 等发表题为 Prenatal development of human immunity 的综述。作者指出, 血液系统和免疫系统在胚胎早期是平行发育的,大规模的单细胞基因组学、成像技术和人类细胞图谱计划共同推动了对胎儿免疫系统发育变化规律的研究。人类早期生命中血液和免疫系统的发育发生在几个解剖部位,主要造血部位由胚外卵黄囊转变为胚内 AGM、肝脏和骨髓。T 细胞的分化和成熟仅限于胸腺。免疫细胞会定位到其他淋巴或外周器官,包括淋巴结、皮肤、肠、肾和肺,并适应相应的器官环境。不同的免疫细胞类型在不同的妊娠阶段发育和成熟,这对于建立基于发育需要的耐受和功能反应是必要的。这为发育中的胚胎和胎儿在怀孕期间和出生后暴露抗原做好了准备。
在特定的发育窗口期,宿主对微生物暴露的适应对于确保器官发育、生长和免疫功能至关重要。母乳是影响新生儿微生物的一个重要因素,母乳通过分泌抗体,乳寡糖或乳蛋白来塑造不稳定的早期肠道菌群。一旦幼儿开始食用固体食物,母乳的这些保护作用就会消失,从而使内生微生物在关键发育窗口期刺激发生「断奶反应」。
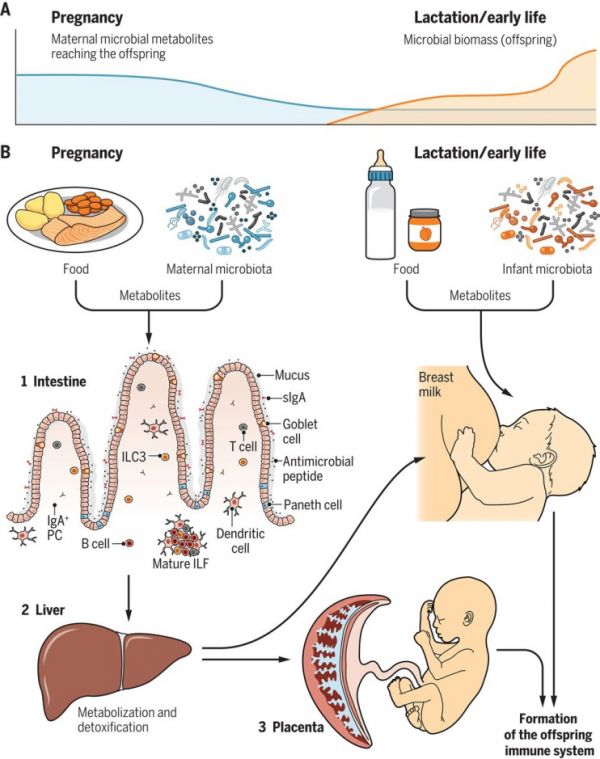 图 4 发育中的胎儿和新生儿暴露于微生物次生代谢物的宿主屏障图片来源:Science 母胎界面抗病毒免疫反应机制第三篇综述是来自耶鲁大学医学院免疫生物学系的 Laura J. Yockey 等研究人员,题为 Contributions of maternal and fetal antiviral immunity in congenital disease。 怀孕期间的病毒感染可能会对妊娠结局、胎儿发育和产妇健康造成毁灭性的后果。在这篇综述中,作者研究了已知的母胎界面抗病毒免疫反应机制,并讨论了当这些机制失效时导致胎儿先天性疾病或慢性病毒感染的可能通路。该综述强调了孕妇免疫激活或怀孕期间病毒感染引发的不受控制的炎症的作用,以及其潜在的病理影响,包括组织损伤和胎儿死亡。作者重点介绍了病毒及其对病毒的免疫反应影响胎盘和胎儿发育的一些分子机制,一方面病毒通过直接感染胎儿带来伤害,另一方面母胎免疫反应也可能会导致胎儿健康受损。探究感染时胎儿和母体免疫反应特点,对未来治疗策略的发展有指导作用。 疫苗接种新策略?母体 - 新生儿二元组第四篇综述 Vaccination strategies to enhance immunity in neonates,本文强调了将母体 - 新生儿二元组为一体来增强新生儿早期的免疫力,新生儿十分容易感染病原体,接种疫苗仍然是目前预防感染的性价比最高的方法之一。但是,当前的疫苗并未针对引起大多数严重新生儿感染的病原体,并且疫苗接种后诱导保护性病原体特异性免疫所花费的时间限制了生命的最初几天至几周内的保护。替代策略包括使用疫苗广泛刺激新生儿的免疫力,或在怀孕期间给孕妇接种疫苗以诱导保护性抗体,这些抗体进而垂直转移至后代。通过整合这些方法可以进一步改善保护,即在垂直转移的母体免疫的掩护下为新生儿接种疫苗,即母体 - 新生儿二元组为一体。
图 4 发育中的胎儿和新生儿暴露于微生物次生代谢物的宿主屏障图片来源:Science 母胎界面抗病毒免疫反应机制第三篇综述是来自耶鲁大学医学院免疫生物学系的 Laura J. Yockey 等研究人员,题为 Contributions of maternal and fetal antiviral immunity in congenital disease。 怀孕期间的病毒感染可能会对妊娠结局、胎儿发育和产妇健康造成毁灭性的后果。在这篇综述中,作者研究了已知的母胎界面抗病毒免疫反应机制,并讨论了当这些机制失效时导致胎儿先天性疾病或慢性病毒感染的可能通路。该综述强调了孕妇免疫激活或怀孕期间病毒感染引发的不受控制的炎症的作用,以及其潜在的病理影响,包括组织损伤和胎儿死亡。作者重点介绍了病毒及其对病毒的免疫反应影响胎盘和胎儿发育的一些分子机制,一方面病毒通过直接感染胎儿带来伤害,另一方面母胎免疫反应也可能会导致胎儿健康受损。探究感染时胎儿和母体免疫反应特点,对未来治疗策略的发展有指导作用。 疫苗接种新策略?母体 - 新生儿二元组第四篇综述 Vaccination strategies to enhance immunity in neonates,本文强调了将母体 - 新生儿二元组为一体来增强新生儿早期的免疫力,新生儿十分容易感染病原体,接种疫苗仍然是目前预防感染的性价比最高的方法之一。但是,当前的疫苗并未针对引起大多数严重新生儿感染的病原体,并且疫苗接种后诱导保护性病原体特异性免疫所花费的时间限制了生命的最初几天至几周内的保护。替代策略包括使用疫苗广泛刺激新生儿的免疫力,或在怀孕期间给孕妇接种疫苗以诱导保护性抗体,这些抗体进而垂直转移至后代。通过整合这些方法可以进一步改善保护,即在垂直转移的母体免疫的掩护下为新生儿接种疫苗,即母体 - 新生儿二元组为一体。 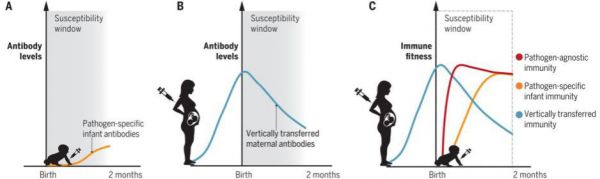
相关知识
“阳过”之后免疫力低?Cell重磅:新冠肺炎破坏人体免疫系统
Science子刊封面论文证实,运动带来是健康益处源于免疫系统
维生素与免疫系统健康
Cell子刊:膳食纤维虽好,摄入也要因人而异
环境污染的健康效应与调控
Cell Research:防御与营养并重:揭示母乳如何塑造婴儿的微生物群和免疫力
《Science》发表北大医学“空气污染与卫生治理”全球综述:现况、挑战与优先行动
Cell Research:防御与营养并重:揭示母乳如何塑造婴儿的微生物群和免疫力@MedSci
《热心肠周刊》第102期
发酵乳调控人体肠道营养健康的研究进展
网址: Cell, Science 特刊——聚焦生命早期免疫系统发展的调控因素和作用机制 https://www.trfsz.com/newsview231046.html
推荐资讯
- 1男女激情后不宜做哪些事 4413
- 2从出汗看健康 出汗透露你的健 3852
- 3早上怎么喝水最健康? 3647
- 4习惯造就健康 影响健康的习惯 3292
- 5五大原因危害女性健康 如何保 3192
- 6连花清瘟、布洛芬等多款感冒药 2960
- 7男子喝水喉咙里像放了刀子一样 2459
- 810人混检核酸几天出结果?1 2225
- 9第二轮新冠疫情要来了?疾控中 2223
- 10转阴多久没有传染性?满足四个 2163