两项小鼠模型的新研究表明肠道菌群从饮食中的色氨酸产生的代谢产物能够调控肠道和中枢神经系统的炎症。
宿主与微生物之间的相互作用是为健康疾病奠定基础的基本成分。维持人类与微生物之间互利共生的一个重要因素是微生物所产生的独特的代谢产物,既为宿主提供了营养同时也参与了免疫系统的发育。组织微环境决定着微生物的组成,所以改变作为细菌能量来源的饮食成分,如糖、脂肪或纤维的摄取,能够影响肠道内微生物的种类。相反,宿主免疫系统的改变,无论是遗传变异还是同时发生的感染,也能够影响肠道微生物。例如,TLR5基因缺陷小鼠由于缺少对鞭毛的免疫应答,肠道内出现多鞭毛细菌爆发。
色氨酸是一种必需氨基酸,通过饮食获得。在本期的Nature Medicine中,两篇报道表明细菌对色氨酸的异化作用产生的代谢产物调控炎症和疾病发展,不仅是在肠道中而且也会影响中枢神经系统。在一篇报道中,Lamas等人发现一种参与调往和抗真菌免疫应答的蛋白CARD9缺陷的小鼠对肠炎易感。并且对肠炎的易感性能够通过移植肠道菌群传染给无菌野生型小鼠。因此宿主遗传缺陷塑造了肠道菌群的组成,从而影响疾病发展。进一步分析肠道菌群揭示了这种疾病促发的肠道菌群缺少能够将色氨酸代谢成AHR配体的细菌,如Lactobacillus reuteri和Allobaculum。
给小鼠补充Lactobacillus菌株能够逆转CARD9缺陷小鼠对肠炎的易感性。作者进一步报道了这些细菌能够将色氨酸异化为吲哚衍生物,如吲哚-3-乙酸和其他已知的AHR配体,促进对肠道健康十分重要的细胞因子IL-22的产生。值得注意的是,给CARD9缺陷小鼠补充IL-22既能够保护小鼠抵抗肠炎同时也能够使AHR配体产生恢复正常,突出了肠道微生物与免疫系统之间双向的相互作用。这个现象似乎不局限于小鼠,因为人类肠炎患者粪便中的AHR配体含量也出现减少。
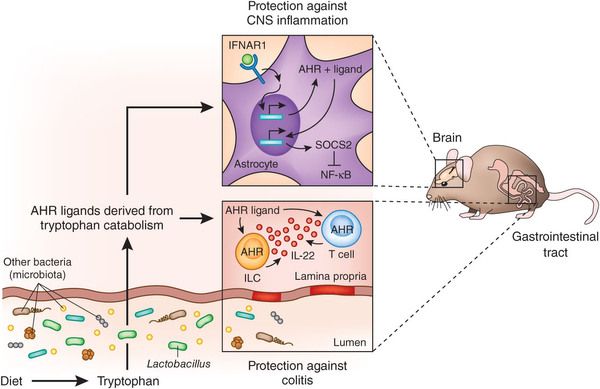
Rothhammer等人则发现色氨酸代谢产物的影响不仅仅局限于肠道,同时也能够调控中枢神经系统的炎症反应。实际上,给小鼠喂色氨酸缺乏的饲料,小鼠出现特别强的中枢神经系统炎症反应,并且这种现象在给小鼠喂养含有色氨酸的饲料后可以恢复。将食物中的色氨酸转化为AHR配体的肠道菌群主要是对氨苄霉素敏感的细菌,因为给小鼠进行氨苄霉素处理会干扰疾病的治疗。值得注意的是,Lamas等人的研究中,L.reuteri同样是氨苄霉素敏感的,并且可能是在色氨酸介导的中枢神经系统炎症保护作用中关键的一员。
综上,Lamas和Rothhammer等人的研究对于揭示中枢神经系统和肠道炎症疾病的机制都做出了重要贡献,并且有助于发展干预治疗相关疾病的新的治疗策略。随着微生物-代谢领域的逐渐成熟,在不远的将来我们可能会见证微生物及代谢产物在健康医疗领域的重大进展。
参考文献:
1. Lamas, B. et al. Nat. Med. 22, 598–605 (2016).
2. Rothhammer, V. et al. Nat. Med. 22, 586–597 (2016).返回搜狐,查看更多
责任编辑:






