糖代谢
糖代谢可分为分解代谢和合成代谢两个方面,生物体内的糖代谢基本过程相类似。糖的分解代谢是指糖类物质分解成小分子物质的过程。糖在生物体内经过一系列的分解反应后,释放出大量的能量,供机体生命活动之用。同时在分解过程中形成的某些中间产物,又可作为合成脂类、蛋白质、核酸等生物大分子物质的原料(作为碳架)。糖的分解代谢可分为无氧代谢和有氧代谢。在无氧条件下,糖的分解通常不完全,此时释放的能量较少,并产生各种代谢产物;在有氧条件下,糖可以被完全氧化,最终生成二氧化碳和水,并释放出大量能量。糖的合成代谢是指生物体将某些小分子非糖物质转化为糖或将单糖合成低聚糖及多糖的过程。这个过程需要供给能量。糖代谢还包括生物体对糖的吸收以及代谢产物的排泄,就微生物而言,这些过程是通过细胞膜来完成的。本章将着重讨论糖的分解代谢 [1]。
血液中的葡萄糖,称为血糖(blood glucose)体内血糖浓度是反映机体内糖代谢状况的一项重要指标。正常情况下,血糖浓度是相对恒定的。正常人空腹血浆葡萄糖糖浓度为3.9~6.1mmol/L(葡萄糖氧化酶法)。空腹血浆葡萄糖浓度高于7.0 mmol/L称为高血糖,低于3.9mmol/L称为低血糖。要维持血糖浓度的相对恒定,必须保持血糖的来源和去路的动态平衡。
血糖代谢
血糖的来源:①食物中的糖是血糖的主要来源;②肝糖原分解是空腹时血糖的直接来源;③非糖物质如甘油、乳酸及生糖氨基酸通过糖异生作用生成葡萄糖,在长期饥饿时作为血糖的来源。
血糖的去路:①在各组织中氧化分解提供能量,这是血糖的主要去路;②在肝脏、肌肉等组织进行糖原合成;③转变为其他糖及其衍生物,如核糖、氨基糖和糖醛酸等;④转变为非糖物质,如脂肪、非必需氨基酸等;⑤血糖浓度过高时,由尿液排出。血糖浓度大于8.9~10.00mmol/(160-180mg/dl),超过肾小管重吸收能力,出现糖尿。将开始出现糖尿时的血糖浓度称为肾糖阈。糖尿病在理想情况下出现,常见于糖尿病患者。
血糖调节
正常人体血糖浓度维持在一个相对恒定的水平,这对保证人体各组织器官的利用非常重要,特别是脑组织,几乎完全依靠葡萄糖供能进行神经活动,血糖供应不足会使神经功能受损,因此血糖浓度维持在相对稳定的正常水平是极为重要的。
正常人体内存在着精细的调节血糖来源和去路动态平衡的机制,保持血糖浓度的相对恒定是神经系统、激素及组织器官共同调节的结果。
 糖代谢相关资料
糖代谢相关资料
神经系统对血糖浓度的调节主要通过下丘脑和自主神经系统调节相关激素的分泌。激素对血糖浓度的调节,主要是通过胰岛素、胰高血糖素、肾上腺素、糖皮质激素、生长激素及甲状腺激素之间相互协同、相互拮抗以维持血糖浓度的恒定。激素对血糖浓度的调节。
肝脏是调节血糖浓度的最主要器官。血糖浓度和各组织细胞膜上葡萄糖转运体(glucose transporters)是器官水平调节的两个主要影响因素,此时细胞膜上葡萄糖转运体家族有GLUT1-5,是双向转运体。在正常血糖浓度情况下,各组织细胞通过细胞膜上GLUT1和 GLUT3摄取葡萄糖作为能量来源;当血糖浓度过高是,肝细胞膜上的GLUT2起作用,快速摄取过多的葡萄糖进入肝细胞,通过肝糖原合成来降低血糖浓度;血糖浓度过高会刺激胰岛素分泌,导致肝脏及肌肉和脂肪组织细胞膜上GLUT4的量迅速增加,加快对血液中葡萄糖的吸收,合成肌糖原或转变成脂肪储存起来。当血糖浓度偏低时,肝脏通过糖原分解及糖异生升高血糖浓度。
从体外实验了解机体对血糖浓度的调节能力,可以通过葡萄糖耐量试验(glucose tolerance test,GTT)获得糖耐量试验曲线加以理解。正常人由于存在精细的调节机制,空腹时正常血糖浓度是3.8-6.1 mmol/L,在口服或静脉注射葡萄糖2小时后血糖浓度<7.8 mmol/L。糖耐量减退病人,一般空腹血糖浓度<7.0 mmol/L,口服或静脉注射葡萄糖0.5-1小时后最高浓度<11.1 mmol/L,2小时血糖浓度≥7.8 mmol/L并且<11.1mmol/L,称为亚临床或无症状的糖尿病,糖耐量试验在这种病人的早期诊断上颇具意义。典型的糖尿病人糖耐量试验为:空腹血糖浓度在6.1-7.0 mmol/L,口服或静脉注射葡萄糖2小时后血糖浓度7.8-11.1 mmol/L,说明病人调节血糖浓度能力降低。临床上建议检测空腹血糖浓度和2小时餐后血糖浓度,简化糖耐量试验过程。
食物中的糖主要是淀粉,另外包括一些双糖及单糖。多糖及双糖都必须经过酶的催化水解成单糖才能被吸收。
食物中的淀粉经唾液中的α-淀粉酶作用,催化淀粉中α-1,4-糖苷键的水解,产物是葡萄糖、麦芽糖、麦芽寡糖及糊精。由于食物在口腔中停留时间短,淀粉的主要消化部位在小肠。小肠中含有胰腺分泌的α-淀粉酶,催化淀粉水解成麦芽糖、麦芽三糖、α-临界糊精和含分支的异麦芽糖。在小肠黏膜刷状缘上,含有α-糊精酶,此酶催化α-极限糊精的α-1,4-糖苷键及α-1,6-糖苷键水解,使α-糊精水解成葡萄糖;刷状缘上还有麦芽糖酶可将麦芽三糖及麦芽糖水解为葡萄糖。小肠黏膜还有蔗糖酶和乳糖酶,前者将蔗糖分解成葡萄糖和果糖,后者将乳糖分解成葡萄糖和半乳糖,有些成人由于乳糖酶缺乏,在食用牛奶后发生乳糖消化吸收障碍,而引起腹胀、腹泻等症状。
 糖代谢
糖代谢
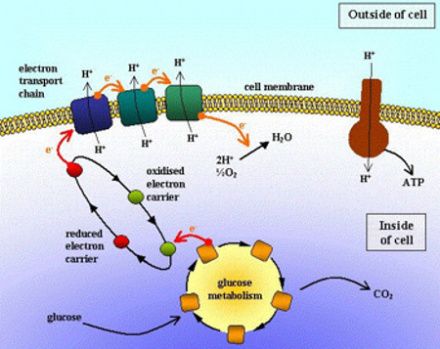
糖被消化成单糖后的主要吸收部位是小肠上段,己糖尤其是葡萄糖被小肠上皮细胞摄取是一个依赖Na+的耗能的主动摄取过程,有特定的载体参与:在小肠上皮细胞刷状缘上,存在着与细胞膜结合的Na+-葡萄糖联合转运体,当Na+经转运体顺浓度梯度进入小肠上皮细胞时,葡萄糖随Na+一起被移入细胞内,这时对葡萄糖而言是逆浓度梯度转运。这个过程的能量是由Na+的浓度梯度(化学势能)提供的,它足以将葡萄糖从低浓度转运到高浓度。当小肠上皮细胞内的葡萄糖浓度增高到一定程度,葡萄糖经小肠上皮细胞基底面单向葡萄糖转运体(unidirectional glucose transporter)顺浓度梯度被动扩散到血液中。小肠上皮细胞内增多的Na+通过钠钾泵(Na+-K+ATP酶),利用ATP提供的能量,从基底面被泵出小肠上皮细胞外,进入血液,从而降低小肠上皮细胞内Na+浓度,维持刷状缘两侧Na+的浓度梯度,使葡萄糖能不断地被转运。
无氧酵解
当机体处于相对缺氧情况(如剧烈运动)时,葡萄糖或糖原分解生成乳酸,并产生能量的过程称之为糖的无氧酵解。这个代谢过程常见于运动时的骨骼肌,因与酵母的生醇发酵非常相似,故又称为糖酵解。反应过程
参与糖酵解反应的一系列酶存在在细胞质中,因此糖酵解的全部反应过程均在细胞质中进行。根据反应特点,可将整个过程分为四个阶段:
一 己糖磷酸化:
⒈ 葡萄糖或糖原磷酸化为6-磷酸葡萄糖(glucose-6-phosphate,G-6-P)
⑴催化葡萄糖生成G-6-P的是己糖激酶(hexokinase,HK),ATP提供磷酸基团,Mg2+作为激活剂。这个反应的ΔG"0 =-16.7KJ/mol,基本是一个不可逆的反应。己糖激酶是糖酵解过程关键酶之一。
己糖激酶广泛存在各组织中,Km为0.1mmol/L,对葡萄糖的亲和力高。哺乳动物中已发现了四种己糖激酶的同工酶Ⅰ-Ⅳ型。Ⅳ型酶只存在于肝脏,对葡萄糖有高度专一性,又称葡萄糖激酶(glucokinase,GK),GK对葡萄糖的Km为10mmol/L,对葡萄糖的亲和力低,这种特性的存在,使GK催化的酶促反应只有在饮食后大量消化吸收的葡萄糖进入肝脏后才加强,生成糖原储存于肝中,在维持血糖浓度恒定的过程中发挥了重要作用。
⑵从糖原开始的分解途径,是糖原在磷酸化酶的作用下成为1-磷酸葡萄糖(G-1-P),再变位成为G-6-P。
 糖代谢
糖代谢
⑶G-6-P是一个重要的中间代谢产物,是许多糖代谢途径(无氧酵解、有氧氧化、磷酸戊糖途径、糖原合成、糖原分解)的连接点。
⑷葡萄糖进入细胞后进行了一系列的磷酸化,其目的在于:磷酸化后的化合物极性增高,不能自由进出细胞膜,因而葡萄糖磷酸化后不易逸出胞外,反应限制在细胞质中进行;同时从ATP中释放出的能量储存到了6-磷酸葡萄糖中;另外结合了磷酸基团的化合物不仅能减低酶促反应的活化能,同时能提高酶促反应的特异性。
2. G-6-P生成6-磷酸果糖(fructose-6-phosphate,F-6-P)
此反应在磷酸己糖异构酶催化下进行,是一个醛-酮异构变化。
⒊ 6-磷酸果糖生成1,6-二磷酸果糖(Fructose l,6 bisphosphate,F-1,6-BP)
催化此反应的酶是6-磷酸果糖激酶1(6-phosphofructokinase1,PFK 1),这是糖酵解途径的第二次磷酸化反应,需要ATP与Mg2+参与,ΔG"0 =-14.2KJ/mol,反应不可逆。
6-磷酸果糖激酶1是糖酵解过程的主要限速酶,是糖酵解过程中的主要调节点。
至此,糖酵解完成了代谢的第一个阶段,这一阶段的主要特点是葡萄糖的磷酸化,并伴随着能量的消耗,糖酵解若从葡萄糖开始磷酸解,则每生成1分子F-1,6-BP消耗了2分子ATP;若从糖原开始磷酸解,则每生成1分子F-1,6-BP消耗1分子ATP。在这一阶段中有二个不可逆反应,从葡萄糖开始由二个关键酶己糖激酶和6-磷酸果糖激酶1催化;从糖原开始由二个关键酶磷酸化酶和6-磷酸果糖激酶1催化,它们是糖酵解过程的调节点。
(二)1分子磷酸己糖裂解为2分子磷酸丙糖
F-1,6-BP裂解为2分子磷酸丙糖,此反应由醛缩酶催化,反应可逆。3-磷酸甘油醛和磷酸二羟丙酮,两者互为异构体,在磷酸丙糖异构酶催化下可互相转变,当3-磷酸甘油醛在继续进行反应时,磷酸二羟丙酮可不断转变为3-磷酸甘油醛,这样1分子F-1,6-BP生成2分子3-磷酸甘油醛。
(三)2分子磷酸丙糖氧化为2分子丙酮酸
1.3-磷酸甘油醛脱氢氧化成为1,3-二磷酸甘油酸
此反应由3—磷酸甘油醛脱氢酶催化脱氢、加磷酸,其辅酶为NAD+,反应脱下的氢交给NAD+成为NADH+H+;反应时释放的能量储存在所生成的1,3-二磷酸甘油酸1位的羧酸与磷酸的构成的混合酸酐内,此高能磷酸基团可将能量转移给ADP形成ATP。
此反应由3-磷酸甘油酸激酶催化,产生1分子ATP,这是无氧酵解过程中第一次生成ATP。由于是1分子葡萄糖产生2分子1,3-二磷酸甘油酸,所以在这一过程中,1分子葡萄糖可产生2分子ATP。ATP的产生方式是底物水平磷酸化(
3.3-磷酸甘油酸转变成2-磷酸甘油酸
此反应由磷酸甘油酸变位酶催化,磷酸基团由3-位转至2-位。
⒋2-磷酸甘油酸脱水生成磷酸烯醇式丙酮酸(phosphoenolpyruvate,PEP)
此脱水反应由烯醇化酶所催化,Mg2+作为激活剂。反应过程中,分子内部能量重新分配,形成含有高能磷酸基团的磷酸烯醇式丙酮酸。
5.磷酸烯醇式丙酮酸转变丙酮酸
此反应由丙酮酸激酶(pyruvate kinase,PK) 催化,Mg2+作为激活剂,产生1分子ATP,ΔG'0=-61.9KJ/mol,在生理条件下,此反应不可逆。丙酮酸激酶也是无氧酵解过程中的关键酶及调节点。
 糖代谢
糖代谢
这是无氧酵解过程第二次生成ATP,产生方式也是底物水平磷酸化。由于是1分子葡萄糖产生2分子丙酮酸,所以在这一过程中,1分子葡萄糖可产生2分子ATP。
反应的第二阶段的特点是能量的产生。无氧酵解过程的能量产生主要在3-磷酸甘油醛脱氢成为1,3-二磷酸甘油酸及磷酸烯醇式丙酮酸转变为丙酮酸过程中,共产生4分子ATP,产生方式都是底物水平磷酸化。这一阶段中丙酮酸激酶是糖酵解过程的另一个关键酶和调节点。
(四)2分子丙酮酸还原为2分子乳酸
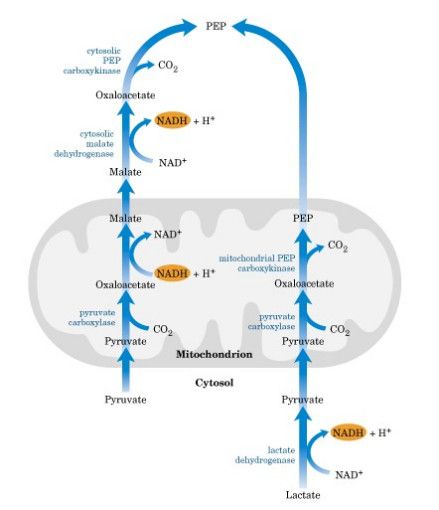
在无氧条件下,丙酮酸被还原为乳酸。此反应由乳酸脱氢酶催化,乳酸脱氢酶有多种同工酶,骨骼肌中主要含有LDH5,它和丙酮酸亲和力较高,有利于丙酮酸还原为乳酸,LDH5的辅酶是NAD+。还原反应所需的NADH+H+是3-磷酸甘油醛脱氢时产生,作为供氢体脱氢后成为NAD+,再作为3-磷酸甘油醛脱氢酶的辅酶。因此,NAD+来回穿梭,起着递氢作用,使无氧酵解过程持续进行。在有氧的条件下,3-磷酸甘油醛脱氢产生的NADH+H+从细胞质中通过穿梭系统进入线粒体经电子传递链传递生成水,同时释放出能量。
能量变化
1分子葡萄糖在缺氧的条件下转变为2分子乳酸,同时伴随着能量的产生,净产生2分子ATP;糖原开始1分子葡萄糖单位糖酵解成乳酸,净产生3分子ATP。
生理意义
(一) 主要的生理功能是在缺氧时迅速提供能量
(二)正常情况下为一些细胞提供部分能量
(三) 糖酵解是糖有氧氧化的前段过程,其一些中间代谢物是脂类、氨基酸等合成的前体。
糖酵调节
糖酵解途径中有3个不可逆反应:分别由己糖激酶(葡萄糖激酶)、6-磷酸果糖激酶1和丙酮酸激酶催化的反应。它们是糖无氧酵解途径的三个调节点,其中以6-磷酸果糖激酶1的活性是该途径中的主要调节点。
(一)己糖激酶活性的别构调节
骨骼肌中的己糖激酶的Km相对较小,在血糖达到一定浓度后,活性就能达到最高,它是一种别构酶,其活性受到自身反应产物6-磷酸葡萄糖的抑制。肝内的葡萄糖激酶的直接调节因素是血糖浓度,由于葡萄糖激酶Km相对较大,在餐后、血糖浓度很高时,过量的葡萄糖运输到肝内,肝内的葡萄糖激酶激活;葡萄糖激酶也是别构酶,活性受到6-磷酸果糖的抑制,而不受6-磷酸葡萄糖的抑制,这样可保证肝糖原顺利合成。
(二)6-磷酸果糖激酶1的别构调节
6-磷酸果糖激酶1是糖酵解途径中最重要的一个调节点,它是别构酶,由4个亚基组成,有很多激活剂和抑制剂。高浓度ATP、柠檬酸是此酶的变构抑制剂。ADP、AMP、2,6-二磷酸果糖(Fructose 2,6 bisphosphate,F-2,6-BP)是此酶的变构激活剂。2,6-二磷酸果糖尽管和1,6二磷酸果糖结构相似,但F-2,6-BP不是6-磷酸果糖激酶1的产物,而是6-磷酸果糖激酶1最强烈的激活剂、最重要的调节因素。
F-2,6-BP的生成是以6-磷酸果糖为底物在6-磷酸果糖激酶2(6-phosphofructokinase2,PFK2)催化下产生(图6-5)。6-磷酸果糖激酶2是双功能酶,包括6-磷酸果糖激酶2与2,6-二磷酸果糖酶2活性,它们同时存在于一条55x103(多肽链中。6-磷酸果糖激酶2的别构激活剂是底物F-6-P,在糖供应充分时,F-6-P激活双功能酶中的6-磷酸果糖激酶2的活性、抑制2,6-二磷酸果糖酶2活性,产生大量F-2,6-BP。相反,在葡萄糖供应不足的情况下,胰高血糖素刺激产生cAMP,激活A激酶,使双功能酶磷酸化后,双功能酶中的6-磷酸果糖激酶2活性抑制而2,6-二磷酸果糖酶2活性激活,减少F-2,6-BP产生。由此可见,在高浓度葡萄糖的情况下,2,6-二磷酸果糖浓度提高,可激活6-磷酸果糖激酶1,促进糖酵解过程进行。F-2,6-BP在参与糖代谢调节中起着重要作用。
(三)丙酮酸激酶
 糖代谢相关书籍
糖代谢相关书籍
丙酮酸激酶是糖酵解过程的第二个调节点,1,6-二磷酸果糖是此酶的别构激活剂,而ATP是该酶的别构抑制剂,ATP能降低该酶对底物磷酸烯醇式丙酮酸的亲和力;乙酰辅酶A及游离长链脂肪酸也是该酶抑制剂,它们都是产生ATP的重要物质。
有氧氧化(aerobicoxidation)是指葡萄糖生成丙酮酸后,在有氧条件下,进一步氧化生成乙酰辅酶A,经三羧酸循环彻底氧化成水、二氧化碳及能量的过程。这是糖氧化的主要方式,是机体获得能量的主要途径。
反应过程
一、葡萄糖氧化生成丙酮酸;
这一阶段和糖酵解过程相似,在细胞质中进行。在缺氧的条件下丙酮酸生成乳酸。在有氧的条件下丙酮酸进入线粒体生成乙酰辅酶A,再进入三羧酸循环。
二、丙酮酸氧化脱羧生成乙酰辅酶A
在有氧条件下,丙酮酸从细胞质进入线粒体。在丙酮酸脱氢酶复合体(pyruvate dehydrogenasecomplex)的催化下进行氧化脱羧反应,该反应的ΔG'0=-39.5kJ/mol,反应不可逆(图6-6)。丙酮酸脱氢酶复合体是由三种酶组成的多酶复合体,它包括丙酮酸脱氢酶,二氢硫辛酸乙酰转移酶及二氢硫辛酸脱氢酶。以乙酰转移酶为核心,周围排列着丙酮酸脱氢酶及二氢硫辛酸脱氢酶。参与的辅酶有TPP,硫辛酸,FAD,NAD+,辅酶A。在多酶复合体中进行着紧密相连的连锁反应过程,反应迅速完成,催化效率高,使丙酮酸脱羧和脱氢生成乙酰辅酶A及NADH+H+。
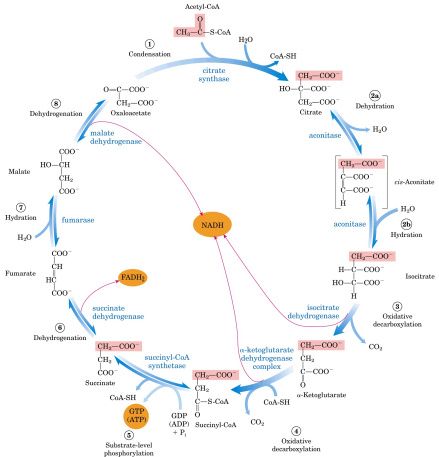
三、三羧酸循环
丙酮酸氧化脱羧生成的乙酰辅酶A要彻底进行氧化,这个氧化过程是三羧酸循环(tricarboxylic acid cycle,TCA cycle)。三羧酸循环是Krebs于1937年发现的。故又称Krebs循环。因为循环中第一个中间产物是柠檬酸,故又称柠檬酸循环(citric acid cycle)。乙酰辅酶A与草酰乙酸缩合生成含有3个羧基的柠檬酸,再经过一系列反应重新变成草酰乙酸完成一轮循环,其中氧化反应脱下的氢经线粒体内膜上经呼吸链传递生成水,氧化磷酸化生成ATP;而脱羧反应生成的二氧化碳则通过血液运输到呼吸系统而被排出,是体内二氧化碳的主要来源。
⒈三羧酸循环反应过程:
⑴乙酰辅酶A与草酰乙酸缩合生成柠檬酸
此反应由柠檬酸合酶(citrate synthase)催化,是三羧酸循环的关键酶,是重要的调节点。由于高能硫酯键水解时释出较多自由能,ΔG'0=-32.2kJ/mol,此反应不可逆。
⑵柠檬酸经顺乌头酸生成异柠檬酸
此反应由顺乌头酸酶催化,柠檬酸脱水、加水生成异柠檬酸。
此反应在异柠檬酸脱氢酶作用下进行脱氢、脱羧,这是三羧酸循环中第一次氧化脱羧。异柠檬酸脱氢酶(isocitrate dehydrogenase)是三羧酸循环的限速酶,是最主要的调节点,辅酶是NAD+,脱氢生成的NADH+H+经线粒体内膜上经呼吸链传递生成水,氧化磷酸化生成3分子ATP。异柠檬酸先脱氢生成草酰琥珀酸,再脱羧生成α-酮戊二酸。ΔG'0=-20.9kJ/mol。
此反应在α-酮戊二酸脱氢酶复合体(α-ketoglutarate dehydrogenase complex)的催化下脱氢、脱羧生成琥珀酰辅酶A,这是三羧酸循环中第二次氧化脱羧。α-酮戊二酸脱氢酶复合体是三羧酸循环的关键酶,是第三个调节点。α-酮戊二酸脱氢酶复合体是多酶复合体,其组成及反应方式都与丙酮酸脱氢酶复合体相似。它所含的三种酶是α-酮戊二酸脱氢酶(需TPP);硫辛酸琥珀酰基转移酶(需硫辛酸和辅酶A);二氢硫辛酸脱氢酶(需FAD、NAD+)。脱氢生成NADH+H+,经线粒体内膜上经呼吸链传递生成水,氧化磷酸化生成3分子ATP。
 糖代谢
糖代谢
由于反应中分子内部能量重排,产物琥珀酰辅酶A中含有一个高能硫酯键,此反应不可逆。ΔG'0=-33.5kJ/mol。
⑸琥珀酰辅酶A转变为琥珀酸
此反应由琥珀酸硫激酶(琥珀酰辅酶A合成酶)催化,琥珀酰辅酶A中的高能硫酯键释放能量,可以转移给ADP(或GDP),形成ATP(或GTP)。细胞中有两种同工酶,一种形成ATP,另一种形成GTP。这是因为琥珀酸硫激酶由α、β亚基组成,α亚基上有磷酸化的组氨酸残基以及结合CoA的位点;β亚基上既可以结合ATP又可以结合GTP。形成的GTP可在二磷酸核苷激酶催化下,将高能磷酸基团转移给ADP生成ATP。这是三羧酸循环中唯一的一次底物水平磷酸化,生成1分子ATP。
⑹琥珀酸脱氢转变为延胡索酸
此反应由琥珀酸脱氢酶催化,辅酶是FAD,脱氢后生成FADH2,经线粒体内膜上经呼吸链传递生成水,氧化磷酸化生成2分子ATP。
⑺延胡索酸转变为苹果酸
⑻苹果酸脱氢生成草酰乙酸
此反应由苹果酸脱氢酶催化,辅酶是NAD+,脱氢后生成NADH+H+,经线粒体内膜上经呼吸链传递生成水,氧化磷酸化生成3分子ATP。
⒉ 三羧酸循环的特点:
⑴三羧酸循环是乙酰辅酶A的彻底氧化过程。草酰乙酸在反应前后并无量的变化。三羧酸循环中的草酰乙酸主要来自丙酮酸的直接羧化。
⑵三羧酸循环是能量的产生过程,1分子乙酰CoA通过TCA经历了4次脱氢(3次脱氢生成NADH+H+,1次脱氢生成FADH2)、2次脱羧生成CO2,1次底物水平磷酸化,共产生12分子ATP。
⑶三羧酸循环中柠檬酸合酶、异柠檬酸脱氢酶、α-酮戊二酸脱氢酶复合体是反应的关键酶,是反应的调节点。
⒊ 三羧酸循环的生理意义
⑴三羧酸循环是糖、脂和蛋白质三大物质代谢的最终代谢通路。糖、脂和蛋白质在体内代谢都最终生成乙酰辅酶A,然后进入三羧酸循环彻底氧化分解成水、CO2和产生能量。
⑵三羧酸循环是糖、脂和蛋白质三大物质代谢的枢纽。
氧化意义
糖有氧氧化的主要功能是提供能量,人体内绝大多数组织细胞通过糖的有氧氧化获取能量。体内l分子葡萄糖彻底有氧氧化生成38(或36)分子 ATP。葡萄糖彻底氧化生成CO2、H2O的过程中,ΔG'0=-2840kJ/mol,生成了38分子 ATP,38×30.5 kJ/mol=1159 kJ/mol,产生能量的有效率为40%左右。
糖的有氧氧化中通过氧化磷酸化反应得到34(或32)分子ATP,通过底物水平磷酸化生成6分子ATP。在肝、肾、心等组织中l分子葡萄糖彻底氧化可生成38分子ATP,而骨骼肌及脑组织中只能生成36分子ATP,这一差别的原因是由于葡萄糖到丙酮酸这阶段的反应是在细胞质中进行,3-磷酸甘油醛脱氢酶的辅酶NADH+H+又必须在线粒体内进行氧化磷酸化,因此NADH+H+要通过穿梭系统进入线粒体,由于穿梭系统的不同,最后获得ATP数目亦不同。从糖原的葡萄糖残基开始氧化,则每分子糖基氧化可形成39(或37)分子ATP。
氧化调节
糖有氧氧化中,葡萄糖生成丙酮酸过程的调节和糖酵解中一样,这里主要讨论丙酮酸脱氢酶复合体和三羧酸循环的调节。
一 丙酮酸脱氢酶复合体的调节
丙酮酸脱氢酶复合体有别构调节和共价调节两种。别构调节的抑制剂有ATP、乙酰辅酶A、NADH、脂肪酸等。激活剂是ADP、CoA、NAD+和Ca2+等。当[ATP]/[ADP],[NADH]/[NAD+]和[乙酰CoA]/[ CoA]很高时,提示能量足够,丙酮酸脱氢酶复合体被别构后活性抑制。
丙酮酸脱氢酶复合体还存在共价修饰调节机制:组成成分之一的丙酮酸脱氢酶中的丝氨酸残基可被特定的磷酸激酶磷酸化而使丙酮酸脱氢酶失活;相应的磷酸酶可使磷酸化的丙酮酸脱氢酶去磷酸化而恢复其活性。这个特定的磷酸激酶又受到ATP的别构激活:当ATP浓度高时,特定的磷酸激酶别构激活,使丙酮酸脱氢酶被磷酸化抑制其活性。
二 三羧酸循环的调节
三羧酸循环的三个调节点是:柠檬酸合酶、异柠檬酸脱氢酶、α-酮戊二酸脱氢酶复合体这三个限速酶,最重要的调节点是异柠檬酸脱氢酶,其次是α-酮戊二酸脱氢酶复合体;最主要的调节因素是ATP和NADH的浓度。当[ATP]/[ADP],[NADH]/[NAD+]很高时,提示能量足够,三个限速酶活性被抑制;反之,这三个限速酶的活性被激活。此外,底物乙酰CoA、草酰乙酸的不足,产物柠檬酸、ATP产生过多,都能抑制柠檬酸合酶。
相互调节
 糖代谢
糖代谢
巴斯德效应(Pastuer effect)是指:在有氧的条件下糖有氧氧化抑制糖无氧酵解。这个效应是Pastuer在研究酵母菌葡萄糖发酵时发现的:在无氧的条件下,糖无氧酵解产生的ATP的速度和数量远远大于有氧氧化,为产生ATP的主要方式。但在有氧的条件下,酵母菌的酵解作用受到抑制。这种现象同样出现在肌肉中:当肌肉组织供氧充分的情况下,有氧氧化抑制糖无氧酵解,产生大量量能量供肌肉组织活动所需。缺氧时,则以糖无氧酵解为主。
在一些代谢旺盛的正常组织和肿瘤细胞中,即使在有氧的条件下,仍然以糖无氧酵解为产生ATP的主要方式,这种现象称为Cratree效应或反巴斯德效应。在具有Cratree效应的组织细胞中,其糖无氧酵解酶系(己糖激酶、6磷酸果糖激酶1、丙酮酸激酶)活性较强,而线粒体中产生ATP的酶系活性较低,氧化磷酸化减弱,以糖无氧酵解酶系产生能量为主。
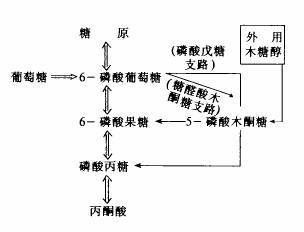
磷酸戊糖途径(pentose phosphate pathway)是葡萄糖氧化分解的另一条重要途径,它的功能不是产生ATP,而是产生细胞所需的具有重要生理作用的特殊物质,如NADPH和5-磷酸核糖。这条途径存在于肝脏、脂肪组织、甲状腺、肾上腺皮质、性腺、红细胞等组织中。代谢相关的酶存在于细胞质中。
反应过程
磷酸戊糖途径是一个比较复杂的代谢途径:6分子葡萄糖经磷酸戊糖途径可以使1分子葡萄糖转变为6分子CO2。磷酸戊糖途径的过程
反应可分为两个阶段:第一阶段是氧化反应,产生NADPH及5-磷酸核糖;第二阶段是非氧化反应,是一系列基团的转移过程。
第一阶段:氧化反应
6-磷酸葡萄糖由6-磷酸葡萄糖脱氢酶(glucose 6-phosphate dehydrogenase,G-6-PD)及6-磷酸葡萄糖酸脱氢酶的催化作用,NADP+是它们的辅酶,G-6-P在第一位碳原子上脱氢脱羧而转变为5-磷酸核酮糖,同时生成2分子NADPH+H+及1分子CO2。5-磷酸核酮糖在异构酶的作用下成为5-磷酸核糖。
在这一阶段中产生了NADPH+H+和5-磷酸核糖这两个重要的代谢产物。
第二阶段:非氧化反应--一系列基团的转移
在这一阶段中磷酸戊糖继续代谢,通过一系列的反应,循环再生成G-6-P。5-磷酸核酮糖经异构反应转变为5-磷酸核糖或5-磷酸木酮糖,三种形式的磷酸戊糖经转酮醇酶催化转移酮醇基(—CO-CH20H)及转醛醇酶催化转移醛醇基(-CHOH-CO-CH20H),进行基团转移,中间生成三碳、七碳、四碳和六碳等的单糖磷酸酯,最后转变成6-磷酸果糖和3-磷酸甘油醛,进一步代谢成为G-6-P。
生理意义
磷酸戊糖途径不是供能的主要途径,它的主要生理作用是提供生物合成所需的一些原料。
(一)提供NADPH+H+
⒈NADPH+H+作为供氢体,参与生物合成反应。如脂肪酸、类固醇激素等生物合成时都需NADPH+H+,所以脂类合成旺盛的组织如肝脏、乳腺、肾上腺皮质、脂肪组织等磷酸戊糖途径比较活跃。
⒉NADPH+H+是加单氧酶体系的辅酶之一,参与体内羟化反应,例如一些药物、毒物在肝脏中的生物转化作用等。
3.NADPH+H+是谷胱甘肽还原酶的辅酶,NADPH使氧化型谷胱甘肽变为GSH,对维持红细胞中还原型谷胱甘肽(GSH)的正常含量起重要作用。GSH能去除红细胞中的H2O2,维护红细胞的完整性:H2O2在红细胞中的积聚,会加快血红蛋白氧化生成高铁血红蛋白的过程,降低红细胞的寿命;H2O2对脂类的过氧化会导致红细胞膜的破坏,造成溶血。
遗传性G-6-PD缺乏的患者,磷酸戊糖途径不能正常进行,造成NADPH+H+减少,GSH含量低下,红细胞易破坏而发生溶血性黄疸。他们常因食用蚕豆而诱发,故称为蚕豆病。
(二)5-磷酸核糖为核苷酸、核酸的合成提供原料。
(三)三碳糖、四碳糖、五碳糖、七碳糖及六碳糖通过磷酸戊糖途径互相转换。
糖原是体内糖的储存形式,主要以肝糖原、肌糖原形式存在。肝糖原的合成与分解主要是为了维持血糖浓度的相对恒定;肌糖原是肌肉糖酵解的主要来源。糖原由许多葡萄糖通过α-1,4-糖苷键(直链)及α-1,6-糖苷键(分支)相连而成的带有分支的多糖(图6-11),存在于细胞质中。
糖原合成(glycogenesis)是由葡萄糖合成糖原的过程。反之,糖原分解(glycogenolysis)则是指肝糖原分解为葡萄糖的过程。糖原合成及分解反应都是从糖原分支的非还原性末端开始,分别由两组不同的酶催化。
糖原合成
糖原合成首先以葡萄糖为原料合成尿苷二磷酸葡萄糖(uridine diphosphate glucose,UDP-Glc),在限速酶糖原合酶(glycogen synthase)的作用下,将UDP-Glc转给肝、肌肉中的糖原蛋白(glycogenin)上,延长糖链合成糖原。其次糖链在分支酶的作用下再分支合成多支的糖原。反应可以分为二个阶段:
第一阶段:糖链的延长
游离的葡萄糖不能直接合成糖原,它必须先磷酸化为G-6-P再转变为G-1-P,后者与UTP作用形成UDP-Glc及焦磷酸(PPi)。UDP-Glc是糖原合成的底物,葡萄糖残基的供体,称为活性葡萄糖。UDP-Glc在糖原合酶催化下将葡萄糖残基转移到糖原蛋白中糖原的直链分子非还原端残基上,以α-1,4-糖苷键相连延长糖链。
第二阶段:糖链分支
糖原合酶只能延长糖链,不能形成分支。当直链部分不断加长到超过11个葡萄糖残基时,分支酶可将一段糖链(至少含有6个葡萄糖残基)转移到邻近糖链上,以α-1,6-糖苷键相连接,形成新的分支(图6-13),分支以α-1,4-糖苷键继续延长糖链。
 糖代谢
糖代谢
糖原蛋白是一个分子质量为37 kDa的蛋白质,它既是糖链延长的引物,又具有酶活性,在糖原合成起始中具有重要作用(图6-15)。①UDP-Glc提供的一个葡萄糖残基和糖原蛋白上的酪氨酸残基进行共价连接,这一步是由糖原蛋白本身具有的糖基转移酶(glucosyltransferase)所催化的。②结合了一个葡萄糖残基的糖原蛋白和糖原合酶一起三者形成一个牢固的复合物,以后的反应都在这个复合物上进行。③UDP-Glc在糖基转移酶催化下提供葡萄糖残基,糖原合酶催化合成,以α-1,4-糖苷键延长,形成7个葡萄糖残基以上的短链。④随着糖链的延长,糖原合酶最终和糖原蛋白分离。⑤在糖原合酶和分支酶的联合作用下完成糖原的合成,糖原蛋白仍然保留在糖原分子中。
糖原合酶是糖原合成的限速酶,是糖原合成的调节点。糖原蛋白每增加一个葡萄糖残基要消耗2分子ATP(葡萄糖磷酸化以及生成UDP-Glc)。
糖原分解
在限速酶糖原磷酸化酶(glycogen phosphorylase)的催化下,糖原从分支的非还原端开始,逐个分解以α-1,4-糖苷键连接的葡萄糖残基,形成G-1-P。G-1-P转变为G-6-P后,肝及肾中含有葡萄糖-6-磷酸酶,使G-6-P水解变成游离葡萄糖,释放到血液中,维持血糖浓度的相对恒定。由于肌肉组织中不含葡萄糖-6-磷酸酶,肌糖原分解后不能直接转变为血糖,产生的G-6-P在有氧的条件下被有氧氧化彻底分解,在无氧的条件下糖酵解生成乳酸,后者经血循环运到肝脏进行糖异生,再合成葡萄糖或糖原。
当糖原分子的分支被糖原磷酸化酶作用到距分支点只有4个葡萄糖残基时,糖原磷酸化酶不能再发挥作用。此时脱支酶发挥作用,脱支酶具有转寡糖基酶和α-1,6-葡萄糖苷酶两个酶活性:转寡糖基酶将分支上残留的3个葡萄糖残基转移到另外分支的末端糖基上,并进行α-1,4-糖苷键连接;而残留的最后一个葡萄糖残基则通过α-1,6-葡萄糖苷酶水解,生成游离的葡萄糖;分支去除后,糖原磷酸化酶继续催化分解葡萄糖残基形成G-1-P。
调节
在肌肉中糖原的合成与分解主要是为肌肉提供ATP;在肝脏,糖原合成、糖原分解主要是为了维持血糖浓度的相对恒定。它们的作用受到肾上腺素、胰高血糖素、胰岛素等激素的影响:肾上腺素主要作用于肌肉;胰高血糖素、胰岛素主要调节肝脏中糖原合成和分解的平衡。糖原合酶与糖原磷酸化酶分别是糖原合成和糖原分解的限速酶,糖原磷酸化酶和糖原合酶的活性不会同时被激活或同时抑制,它们可以通过别构调节和共价修饰调节两种方式进行活性的调节。
(一) 糖原磷酸化酶活性调节
糖原磷酸化酶以a、b两种形式存在。在糖原磷酸化酶激酶及ATP存在下,在糖原磷酸化酶b的丝氨酸残基进行磷酸化修饰,使无活性的糖原磷酸化酶b转变成有活性的糖原磷酸化酶a。糖原磷酸化酶a可经磷蛋白磷酸酶作用使其丝氨酸残基脱去磷酸,成为无活性的糖原磷酸化酶b。
在肌肉剧烈运动时,糖原磷酸化酶的活性是受到肾上腺素的调节。肾上腺素通过信号转导系统使cAMP的浓度提高,激活A激酶使无活性的糖原磷酸化酶激酶b磷酸化成为有活性的糖原磷酸化酶激酶a,糖原磷酸化酶激酶a进一步使无活性的糖原磷酸化酶b成为有活性的糖原磷酸化酶a,促进糖原分解,产生能量。
当肌肉剧烈运动时,肌糖原分解增加,这过程也涉及是二个别构调节机制。一个是Ca2+的别构调节:Ca2+是肌肉运动的信号,它结合并别构糖原磷酸化酶激酶b使其具有活性,促进无活性的糖原磷酸化酶b转变为有活性的糖原磷酸化酶a。另一个是AMP和ATP的别构调节:AMP在剧烈运动的肌肉中积聚,别构激活糖原磷酸化酶;当ATP足够时,ATP和别构位点结合,使糖原磷酸化酶失活。
在肝脏中,糖原磷酸化酶的活性调节主要受胰高血糖素调节,当血糖浓度降低到一定程度,通过胰高血糖素形成cAMP,激活A激酶使磷酸化酶激酶b成为磷酸化酶激酶a,催化无活性的磷酸化酶b转变为有活性的磷酸化酶a,促使肝糖原分解成葡萄糖释放到血液中,达到升血糖目的。在肝脏中糖原磷酸化酶的活性也存在着别构调节机制。当血糖浓度恢复正常,葡萄糖进入肝细胞并和糖原磷酸化酶a的别构位点结合,使糖原磷酸化酶a上磷酸化的丝氨酸残基暴露给糖原磷酸化酶a磷酸酶,糖原磷酸化酶a脱磷酸成无活性的糖原磷酸化酶b,此时葡萄糖是别构剂。
(二)糖原合成酶活性的调节
糖原合酶也分为a、b两种形式。糖原合酶a具有活性。糖原合酶a被磷酸化转变成无活性的糖原合酶b。在磷蛋白磷酸酶的作用下,无活性的糖原酶b脱磷酸转变为有活性的糖原合酶a。糖原磷酸化酶和糖原合酶的活性在磷酸化与去磷酸化作用下相互调节,一个酶被激活,另一个酶活性被抑制,二个酶不会同时被激活或同时抑制。
糖原磷酸化酶激酶a、糖原磷酸化酶a和糖原合酶b,它们的脱磷酸均由磷蛋白磷酸酶催化。磷蛋白磷酸酶可与磷蛋白磷酸酶抑制物结合而失去活性,以保证糖原磷酸化酶激酶a、糖原磷酸化酶a和糖原合酶b维持磷酸化的状态。只有磷酸化的磷蛋白磷酸酶抑制物才能和磷蛋白磷酸酶结合而使磷蛋白磷酸酶失去活性。因此cAMP激活A激酶,不仅促进糖原磷酸化酶激酶b磷酸化成为糖原磷酸化酶激酶a、磷酸化酶b磷酸化成为磷酸化酶a,又通过磷蛋白磷酸酶抑制剂的磷酸化,达到抑制磷蛋白磷酸酶对糖原磷酸化酶激酶a、糖原磷酸化酶a和糖原合酶b脱磷酸化的目的,最终促进糖原分解,抑制糖原合成。
中酶的磷酸化与去磷酸化使酶活性相应改变,构成一组连续的、级联式(cascade)的酶促反应过程,各级反应不仅都可被调节,而且有放大效应。这种调节机制有利于机体针对不同生理状况作出反应。
贮积病
糖原贮积病(glycogen storage disease)是一类遗传性疾病,表现为异常种类和数量的糖原在组织中沉积,产生不同类型的糖原贮积病,每种类型表现为糖原代谢中的一个特定的酶缺陷或缺失而使糖原贮存,由于肝脏和骨骼肌是糖原代谢的重要部位,因此是糖原贮积病的最主要累及部位.肝脏、肌肉。
糖异生作用(gluconeogenesis)是指非糖物质如生糖氨基酸、乳酸、丙酮酸及甘油等转变为葡萄糖或糖原的过程。糖异生的最主要器官是肝脏。
反应过程
糖异生反应过程基本上是糖酵解反应的逆过程。由于糖酵解过程中由己糖激
酶、6-磷酸果糖激酶1及丙酮酸激酶催化的三个反应释放了大量的能量,构成难以逆行的能障, 因此这三个反应是不可逆的。这三个反应可以分别通过相应的、特殊的酶催化,使反应逆行(图6-19),完成糖异生反应过程。
(一)丙酮酸转变为磷酸烯醇式丙酮酸
丙酮酸生成磷酸烯醇式丙酮酸的反应包括丙酮酸羧化酶和磷酸烯醇式丙酮酸羧激酶催化的两步反应,构成一条所谓“丙酮酸羧化支路”使反应进行。这个反应是糖酵解过程中丙酮酸激酶催化的磷酸烯醇式丙酮酸生成丙酮酸的逆过程。
⒈ 丙酮酸羧化生成草酰乙酸
此反应由丙酮酸羧化酶催化,辅酶是生物素, ATP、Mg2+(Mn2+)参与羧化反应, CO2通过生物素使丙酮酸羧化生成草酰乙酸。此酶存在于线粒体中,故丙酮酸必须进入线粒体才能被羧化为草酰乙酸,这也是体内草酰乙酸的重要来源之一。
2.草酰乙酸脱羧生成磷酸烯醇式丙酮酸(PEP)
此反应由磷酸烯醇式丙酮酸羧激酶催化,由GTP提供能量,释放CO2。
磷酸烯醇式丙酮酸羧激酶在人体的线粒体及胞液中均有存在。存在于线粒体中的磷酸烯醇式丙酮酸羧激酶,可直接催化草酰乙酸脱羧生成PEP,PEP从线粒体转运到细胞质,通过糖酵解逆行过程生成1,6-二磷酸果糖。存在于细胞质中的磷酸烯醇式丙酮酸羧激酶,首先要使草酰乙酸从线粒体转运到细胞质中:由于草酰乙酸不能自由进出线粒体内膜,因此草酰乙酸先要在线粒体内还原生成苹果酸或经转氨基作用生成天冬氨酸;苹果酸、天冬氨酸都能自由进出线粒体内膜,可从线粒体到达细胞质;在细胞质中苹果酸可脱氢氧化、天冬氨酸可再经转氨基作用生成草酰乙酸,完成了将草酰乙酸从线粒体转运到细胞质的过程。然后,转运到细胞质中的草酰乙酸可在磷酸烯醇式丙酮酸羧激酶催化下脱羧生成PEP。
(二)1,6-二磷酸果糖转变为6-磷酸果糖
此反应由1,6-二磷酸果糖酶1催化进行。这个反应是糖酵解过程中1,6-二磷酸果糖酶1催化6-磷酸果糖生成1,6-二磷酸果糖的逆过程。
(三)6-磷酸葡萄糖转变为葡萄糖
此反应由葡萄糖-6-磷酸酶催化进行。这个反应是糖酵解过程中己糖激酶催
化葡萄糖生成6-磷酸葡萄糖的逆过程。
生理意义
⒈糖异生最重要的生理意义是在空腹或饥饿情况下维持血糖浓度的相对恒定
⒉乳酸再利用:
乳酸大部分是由肌肉和红细胞中糖酵解生成的,经血液运输到肝脏或肾脏,经糖异生再形成葡萄糖,后者可经血液运输回到各组织中继续氧化提供能量。这个过程称为是乳酸循环或Cori循环(lactate cycle or Cori cycle)。在安静状态下产生乳酸的量甚少,此途径意义不大。但在某些生理或病理情况下,如剧烈运动时,肌糖原酵解产生大量乳酸,大部分可经血液运到肝脏,通过糖异生作用合成肝糖原或葡萄糖以补充血糖,而血糖又可供肌肉利用。乳酸循环可避免损失乳酸以及防止因乳酸堆积引起的酸中毒。
⒊糖异生促进肾脏排H+、缓解酸中毒
酸中毒时H+能激活肾小管上皮细胞中的磷酸烯醇式丙酮酸羧激酶,促进糖异生进行。由于三羧酸循环中间代谢物进行糖异生,造成α-酮戊二酸含量降低,促使谷氨酸和谷氨酰胺的脱氨生成的α-酮戊二酸补充三羧酸循环,产生的氨则分泌进入肾小管,与原尿中H+结合成NH4+,对H+过多起到缓冲作用,可缓解酸中毒。
异生调节
糖异生途径中四个关键酶催化的反应是糖异生的主要调节点。糖异生与糖酵解是两条相同但方向相反的代谢途径,因此它们必须是互为调节的,两条代谢途径中关键酶的激活或抑制要互相配合:当糖供应充分时,糖酵解有关的酶活性增高,糖异生有关的酶活性减低;当糖供应不足时,糖酵解有关的酶活性减低,糖异生有关的酶活性增高。体内通过改变酶的合成速度、共价修饰调节和别构调节来调控这两条途径中关键酶的活性,以达到最佳生理效应。
⒈ 诱导、抑制关键酶的合成
当血糖浓度升高,一方面可导致胰岛素分泌增加,成为增加糖酵解关键酶合成的诱导因素;另一方面可抑制糖皮质激素和胰高血糖素诱导产生糖异生的关键酶。
⒉ 关键酶的共价修饰调节
当血糖浓度的降低,可导致胰高血糖素、少量的肾上腺素产生,通过cAMP达到抑制糖酵解、增加糖异生的目的。cAMP浓度的增加可使A激酶对丙酮酸酸激酶进行磷酸化,磷酸化后的丙酮酸激酶活性降低,糖酵解过程抑制。胰高血糖素和肾上腺素对6-磷酸果糖激酶2也有共价修饰作用,根据糖供应的情况产生相应的2,6-二磷酸果糖的量,进而影响6-磷酸果糖激酶1的活性,达到调节糖酵解的目的。
⒊ 关键酶的别构调节
⑴乙酰CoA作为别构剂的作用:激活糖异生的丙酮酸羧化酶,抑制糖有氧氧化中的丙酮酸脱氢酶复合体的活性,促进糖异生作用。当细胞能量足够时,三羧酸循环被抑制、乙酰CoA堆积,进而抑制丙酮酸脱氢酶复合体的活性,减缓丙酮酸生成乙酰CoA;与此同时丙酮酸羧化酶激活,增加糖异生过程,将多余的丙酮酸生成葡萄糖。
⑵AMP、ATP作为别构剂的作用:AMP是糖异生的1,6-二磷酸果糖酶1的别构抑制剂,是糖酵解中6-磷酸果糖激酶1的别构激活剂。ATP、柠檬酸是6-磷酸果糖激酶1的别构抑制剂。这二个酶相互协调共同调节糖异生、糖酵解。肝细胞内ATP/ADP比值增加时,糖异生加强而糖酵解被抑制,反之,当ATP/ADP比值下降时,糖酵解加速,而糖异生被抑制。
⑶2,6-二磷酸果糖作为别构剂的作用:2,6-二磷酸果糖在糖酵解、糖异生的相互调节中起着重要作用。2,6-二磷酸果糖是6-磷酸果糖激酶1最强烈的别构激活剂,同时也是1,6-二磷酸果糖酶1的别构抑制剂。在糖供应充分时,2,6-二磷酸果糖浓度增高激活6-磷酸果糖激酶1,抑制1,6-二磷酸果糖酶1,促进糖酵解。在糖供应缺乏时 ,2,6二磷酸果糖浓度降低,减低对6-磷酸果糖激酶1的激活、减低对1,6-二磷酸果糖酶1的抑制,糖异生增加 [2]。
相关知识
糖皮质激素引起糖代谢紊乱
糖类代谢和与人体健康.ppt
糖果代谢与健康说课.ppt
代谢
代谢慢的人怎么提高代谢
代谢概述
代谢调节
物质代谢
新陈代谢
脂肪代谢
网址: 糖代谢 https://www.trfsz.com/newsview327889.html
推荐资讯
- 1男女激情后不宜做哪些事 3842
- 2从出汗看健康 出汗透露你的健 3826
- 3早上怎么喝水最健康? 3623
- 4习惯造就健康 影响健康的习惯 3277
- 5五大原因危害女性健康 如何保 3177
- 6连花清瘟、布洛芬等多款感冒药 2953
- 7男子喝水喉咙里像放了刀子一样 2451
- 810人混检核酸几天出结果?1 2221
- 9第二轮新冠疫情要来了?疾控中 2215
- 10转阴多久没有传染性?满足四个 2159






