浅谈美国医药市场的准入和定价体系
此前,信迪利单抗(Sintimilab)在美国的上市申请结果受到医药行业人士的高度关注。礼来制药公司在美国食品药品监督管理局(FDA)的肿瘤药物专家委员会会议(ODAC会议)表决后发表声明,称“我们曾希望能够通过大胆的定价策略,让Sintilimab为美国患者和医疗系统做出积极的贡献”。那么礼来对Sintilimab的定价策略到底有多么大胆?
礼来公司发言人公开表示如果该药物获得批准,则计划为 Sintilimab的Wholesale Acquisition Cost (WAC)提供与目前市场上的其他PD-1/PD-L1药品相比大约 40% 的折扣。显然,ODAC会议的审评审批结果向行业表明,低定价策略并不是FDA专家们考量的重点,也无法有效影响药物审评决策。
然而,本篇文章依然想要讨论低定价策略在美国市场的有效性,换言之,打六折进入美国市场就能获得商业上的成功吗?并借此机会,以Sintilimab的市场准入为线索,串联介绍一下美国医药市场的准入和定价体系。
从信迪利单抗出海看美国医药市场的准入和定价体系 | 原文标题
华人抗体 | 来 源
Leyla Jiang | 作 者
Dara | 编 辑
01、美国医药市场的整体构成
美国医药市场可以大概理解为由政府支付方市场(government payer market)和商业保险支付方市场 (commercial payer market)组成。
政府支付方市场主要包括Medicare和Medicaid。Medicare是覆盖65岁以上人群的美国联邦健康保险,同时也覆盖部分65岁以下的残疾人和全年龄段的终末期肾病患者。Medicaid是覆盖符合条件的低收入成年人、儿童、孕妇、老年人和残疾人的保险,由各州州政府和联邦政府共同出资。
商业保险支付方市场主要包括Medicare Advantage和雇主为员工购买支付的保险(employer health insurance)。Medicare Advantage,也叫Part C或者MA plans,由 Medicare 批准的商业保险公司承办,必须遵守 Medicare 制定的规则。雇主为员工购买的保险基本上也都是由商业保险公司承办。
面对这样的市场结构,医药企业制定市场化策略最关键的第一步,就是判断产品的患者人群被哪个支付方市场覆盖?
以Sintilimab举例,从概率上讲65岁以上人群癌症患者更多,并且非小细胞肺癌的发病率并没有与收入水平呈明显相关性。此外,65岁以下癌症患者人群主要由雇主为员工购买的商业保险覆盖。
所以大概可以认为Sintilimab的患者群体既涉及政府支付方市场——Medicare,也涉及商业支付方市场。企业一般需要精确到百分比,用以制定更加针对性的策略。
为了理解Sintilimab面临的政府支付方市场,首先要理解Medicare中的两个重要概念:Part B和Part D。
对药品准入而言,Part B与Part D 有完全不同的市场规则。
Part B也叫medical benefit,官方定义为医疗必要服务,即诊断或治疗患者所必需的服务或用品。需要注意的是,Part B也包含药品,具体指需要医生来进行药物注射的药品,一般包括静脉注射产品以及药品处方说明书(FDA label)里明确规定需要医生注射的皮下给药。
Part D即pharmacy benefit,也叫药品福利,具体指美国医保局(Centers for Medicare & Medicaid Services / CMS)报销的处方药药品目录。Part D包含的处方药品一般是口服药以及药品处方说明书里提到可以患者自行注射的皮下给药。
Sintilimab是大分子抗体药,需要到医院或者诊所由医生来进行静脉注射,属于Part B市场。而说到Sintilimab面临的商业支付方市场,美国市场出现的新型趋势是商业保险支付方为了控制费用把昂贵的大分子抗体药从医院引流到特药药房,也称white bagging,这里不做讨论。
02、美国市场准入核心流程
在美国,大多数Part B产品的报销流程称为Buy-and-Bill,医院或者诊所先购买、储存产品 ,然后将产品注射给需要的患者。在患者接受药物和其他医疗护理后,医院或者诊所向支付方提交报销账单。因为报销是在医院或者诊所购买和使用药物之后发生,所以称作buy-and-bill。
美国医保局CMS每年会更新Part B药品的Average Sales Price (ASP),政府支付方对Part B药品的支付价格为ASP+6% (美国政府Sequestration期间由6%调整为4.3%,这里不做具体讨论),商业保险支付方一般会支付高于政府支付的价格。
那么,一个新上市的药品报销的流程是怎样的呢?对于Part B药品来说,上市后准入报销流程大致包括 (补充生物制剂许可申请sBLA不适用于以下流程):
第一步:申请BLA,即生物制剂上市许可。
第二步:申请药品J代码(J-code),这一代码主要用于非口服药物、吸入溶液、化疗和免疫抑制药物,是供医院和其他为医疗保险计费专业人员(coders)在报销过程中使用的“药品社保号”。上市使用两个季度后,美国医保局会生成该药品的ASP (在没有生成ASP之前使用Wholesale Aquisiton Cost/WAC价格报销)。
第三步:政府支付方报销价格为ASP+6%,商业保险支付方通常报销价格更高。
在这样的报销流程下,打了六折的PD-1对医院和诊所到底有多少吸引力呢?总体而言,社区诊所倾向于更多地关注医疗总成本,即提供给患者全流程的药物和服务总成本,假设临床有效性一致的情况下,便宜的产品有助于降低医疗总成本,所以更具有吸引力。
然而大型医院系统更倾向于通过集团采购组织(Group Purchasing Organization / GPO)打包购买更大范围的产品,所以导致对某单一产品的价格敏感性较低。因而,Sintilimab的低定价策略能否成功的一个关键因素取决于其美国市场准入重点客户团队能拿下多少社区肿瘤诊所。(340B医院这里不做讨论。)
03、美国Part B市场中的定价难题 到底是保WAC还是ASP?
通过上文介绍的准入流程我们可以发现,美国药品市场里有两个核心的价格概念,即 Wholesale Acquisition Cost (WAC)以及Average Sales Price (ASP)。
WAC是药企在向批发商(Wholesaler)销售时设定的产品价格。
ASP 是基于市场的价格,反映了产品所有销售价格的加权平均值,其中包括药企与药品福利管理(Pharmacy benefit managers/PBM)、集团采购组织(GPO)、连锁医院系统等等私下协商的所有回扣与折扣(不包含Medicaid折扣)。
通常情况下WAC与ASP的关系此消彼长, 高WAC通常意味着要给购买方很多折扣与回扣,因此会降低ASP价格,而低ASP则会影响政府支付方的支付价格——药王Humira的经典定价模式就是高WAC加高回扣。
另一种定价思路是低WAC搭配低的回扣,这样ASP会保持在一个较高的价格。然而,低WAC并且不提供或者提供很低的回扣策略能否有效执行?执行难度又有多大?
近些年美国医疗市场中出现了多宗大型并购,实现了上下游的垂直整合,即商业医疗保险公司、药品福利管理、特药药房以及集团医院的高度整合。如今美国80%的PBM市场被三大集团控制:CVS-Aetna、Cigna-Express Scripts 和 UnitedHealth-OptumRx。
垂直整合之后,商业保险支付方和PBM有了更大的议价能力,并且在药品使用和医疗费用支出方面的掌控力也大大提升,各种限制管理药物使用以及护理治疗场所的举措给药企带来极大的挑战。在这样的大环境下,支付方议价能力越来越强,药企还剩多少讨价还价的空间?
当然,不同产品的竞争格局不同,准入策略总是要具体情况具体分析。不过总体而言,低WAC定价策略有风险,如何在制定低WAC的同时控制回扣,从而保住高ASP,对商业化团队是个不小的考验。
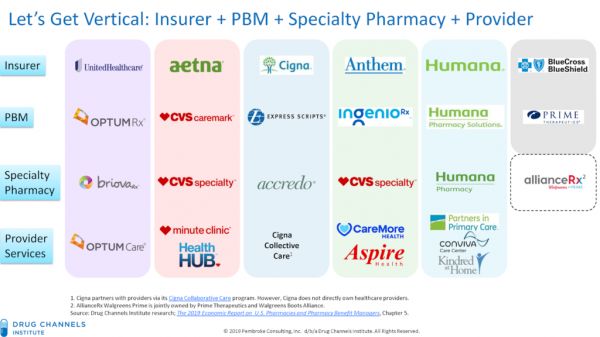
图片来源:Drug Channels Institute
epilogue 结 语
业内人士经常用“九死一生”来形容医药创新的难度,现在看来,对药企来说,市场准入商业化的难度也不低于“九死一生”,并且未来创新产品的定价压力只增不减。随着人口老龄化以及平均寿命的提升,各个国家都面临着医疗健康公共支出可负担性的难题,控费的趋势日益凸显。
目前在核心医药市场,业内人士普遍观察到的现象是创新药物面临比以前更大的市场准入和定价压力。拿笔者的项目经验举例,某跨国药企医学部得知了临床二期振奋人心的实验结果,市场部向公司高层展示了非常乐观以及可观的市场规模预测,然而市场准入部门却提出了“不合时宜”的悲观看法,究其根本原因,在于支付方和专注研发的科学家是基于两套不同的思维体系来理解创新的价值。
应对“九死一生”的挑战需要集体智慧,对于公司寄予厚望的重磅产品,市场准入团队一般在产品早期就开始介入,测试不同国家支付方对产品目前clinical profile的反应,比如临床实验如何设计才能让欧洲市场支付方认可,以及定价区间在哪等等问题。
路漫漫其修远兮,吾将上下而求索。中国创新药出海的风帆已经扬起,如万里博士在华人抗体协会刊登的上一篇文章所说“信达/礼来这次与FDA的ODAC会议长期来看肯定会对中国生物制药公司的国际化和成功出海起到促进的作用,成为中国创新药发展历史上的一个重要里程碑”。
衷心祝愿中国生物制药公司能够以卓越的勇气、前瞻的视野和精准的策略应对海外市场的挑战,在全球范围内建立商业化能力,将中国创造的成果带给世界各地的患者。
原文发布于 2022年2月28日
作者介绍

Leyla Jiang
全球市场定价和市场准入咨询顾问
Leyla Jiang,天津人,目前定居美国华盛顿特区。Leyla Jiang拥有在多国市场的工作经验,广泛涉猎全球主要市场的市场准入和定价体系,对美国、欧洲五国和中国市场有深入的理解和丰富的项目经验。在中国市场曾担任过咨询顾问,也曾在医药企业的市场准入部门任职,兼具行业视野和企业视角。
美国市场的项目经验主要包括肿瘤产品在创新支付模式Oncology Care Model下的定价和准入策略以及住院支付报销体系(Inpatient Prospective Payment System / IPPS)下的创新产品准入策略比如MS-DRG系统下的新技术补贴(New Add-on Technology Payment / NTAP)等等。目前主要关注创新靶点与治疗方法在欧洲市场的准入和定价。
如对文章有任何问题,欢迎联系我一起交流学习。邮箱:leyla.j.jiang@gmail.com。
*特别感谢王星特女士对文本措辞的润色 *The above content reflects the personal viewpoint of the author and not the previous and current organizations that she is affiliated with.
参考文献
[1]https://investor.lilly.com/news-releases/news-release-details/lilly-statement-sintilimab-oncologic-drugs-advisory-committee
[2]https://www.fiercepharma.com/pharma/lilly-and-innovent-s-china-trial-not-diverse-enough-to-apply-to-u-s-approval-for-lung-cancer
[3]https://www.cms.gov/medicare/medicare-part-b-drug-average-sales-price/2022-asp-drug-pricing-files
[4]https://www.pbgh.org/despite-claims-vertical-integration-isnt-great-for-health-care-consumers-or-purchasers/
声 明
文章内容仅供参考,不构成投资建议。投资者据此操作,风险自担, 关于对文中陈述、观点判断保持中立,不对所包含内容的准确性、可靠性或完整性提供任何明示或暗示的保证。请读者仅作参考,并请自行承担全部责任;
本公众号发布的各类文章重在分享,如有侵权请联系我们,我们将会处理。
本文由“健康号”用户上传、授权发布,以上内容(含文字、图片、视频)不代表健康界立场。“健康号”系信息发布平台,仅提供信息存储服务,如有转载、侵权等任何问题,请联系健康界(jkh@hmkx.cn)处理。
相关知识
经验浅谈:天津正规男科医院评价怎么样
中俄人才培养与市场准入研讨会举办 促进两国医药健康产业深度合作
减肥药诺和盈国内获批 国内外药企竞速健康潜力市场
浅谈环境污染与人体健康
医美光电器械市场、产品和公司盘点
移动医疗重构医疗价值体系,市场规模已突破200亿
美体塑形市场即将步入万亿市场?
浅谈健康管理软件价值与功能概述
颜值驱动经济,2000亿国内市场,轻医美注射填充原料市场竞争
医药局约谈后,救命药降价!专家:要从源头上解决保供稳价
网址: 浅谈美国医药市场的准入和定价体系 https://www.trfsz.com/newsview425728.html
推荐资讯
- 1从出汗看健康 出汗透露你的健 3873
- 2早上怎么喝水最健康? 3659
- 3习惯造就健康 影响健康的习惯 3303
- 4五大原因危害女性健康 如何保 3208
- 5连花清瘟、布洛芬等多款感冒药 2965
- 6男子喝水喉咙里像放了刀子一样 2465
- 710人混检核酸几天出结果?1 2229
- 8第二轮新冠疫情要来了?疾控中 2227
- 9转阴多久没有传染性?满足四个 2163
- 10补肾吃什么 补肾最佳食物推荐 2113