Nat Med
环境污染暴露通过呼吸道菌群紊乱影响呼吸健康指标
The airway microbiome mediates the interaction between environmental exposure and respiratory health in humans
Article,2023-06-22
Nature Medicine [IF: 87.245]
DOI:https://doi.org/10.1038/s41591-023-02424-2
文章链接: https://www.nature.com/articles/s41591-023-02424-2
北京时间2023年6月22日晚23时,华南师范大学王璋团队,广东省疾控中心林立丰、孙九峰团队,广州医科大学附属第一医院—广州呼吸健康研究院关伟杰团队合作,在Nature Medicine杂志以长文(Article)发表了题为《人体呼吸道菌群介导环境污染暴露与呼吸健康的相互作用》(The airway microbiome mediates the interaction between environmental exposure and respiratory health in humans)的研究论文(图1)。
环境污染暴露影响呼吸健康,导致肺功能下降与呼吸系统疾病的发生,对全球公共卫生造成重大威胁。健康人体下呼吸道存在微生物群落(呼吸道菌群),其可受环境污染暴露发生改变,并对人体呼吸健康产生影响。尽管污染暴露影响人体肠道菌群,对于人体呼吸道这一直接与环境刺激物相接触部位的菌群特征,及其与环境暴露及呼吸健康的关系仍知之甚少。
慢性阻塞性肺疾病(慢阻肺)是全球及我国重大慢病。不可逆的气道阻塞和肺功能下降是慢阻肺的诊断标准。但环境污染暴露所导致的肺损伤可能早于慢阻肺发生。部分人群肺功能正常但具有污染暴露史和呼吸道症状,其具有发展为慢阻肺的较高风险。识别早期慢阻肺发生发展的微生物群落变化可为疾病防治政策的制定提供参考。
明确疾病状态下呼吸道菌群的变化需要建立一个健康人群的呼吸道菌群基线,但健康人群下呼吸道样本采集的困难性较大,为规模开展呼吸道菌群研究带来挑战。作为一种非入侵手段,诱导痰是目前最可行的规模性获取呼吸道菌群样本的手段之一,但它有多大程度能代表下呼吸道仍不确切。在这项研究中,我们依托2019年广东省居民慢性阻塞性肺疾病(慢阻肺)流行病学调查项目,对广东省6个城市/地区,18个社区,36个居委会,共3,800余居民进行了问卷调查、肺功能检查、身体测量、并进行了诱导痰样本的采集。我们通过大规模人群呼吸道菌群多组学分析,揭示了环境污染暴露、呼吸道菌群与呼吸健康的关系。
呼吸道菌群的地域差异
通过对诱导痰样本进行了严格的质控及微生物组分析,我们总共获取了呼吸道细菌16S rRNA基因扩增子1,651例、真菌ITS扩增719例、宏基因组1,128例,对宏基因组数据进行了物种谱、功能谱、抗生素抗性基因(图1)。我们发现在所有的环境和宿主因素中,地理区域显著贡献了呼吸道微生物群落的变化,其Adonis R2值比排名第二的环境因子(吸烟史)高出10.9倍。同时,个体呼吸道菌群差异随着居民所居住行政区划的差异性(同一个居委会、同一个社区、同一个地区、不同地区)增加而增加,但却同地理距离无明显关系。25个宿主与环境因素同地域显著相关,方差分解分析发现13.1-57.8%的菌群地域差异可被这25个宿主及环境因素所解释,提示呼吸道菌群的地域差异可能同地域相关的环境及人口学因素有关。
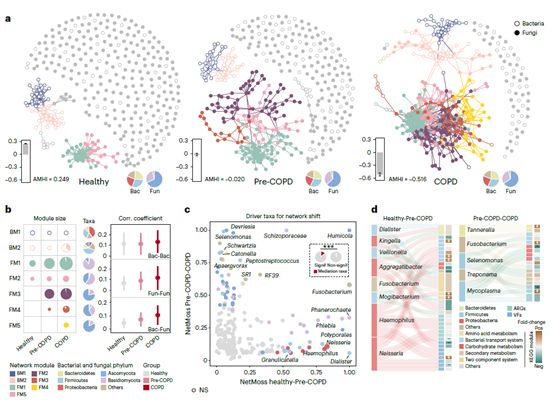
图1. 呼吸道菌群概况及地域差异
(a)研究总体设计与技术路线;(b)宿主及环境因子同呼吸道菌群关联的Adonis分析;(c)居住在同一居委会、同一社区、同一地区与不同地区的居民呼吸道菌群Bray-Curtis距离;(d)呼吸道菌群与地域相关宿主及环境因子的方差分解分析。
呼吸道菌群介导环境污染暴露对肺功能及呼吸道症状的影响
1,393个菌群特征与环境暴露因素(吸烟、二手烟、PM2.5浓度、职业暴露、生物燃料暴露)、肺功能以及呼吸道症状之间具有显著关联。其中1,311个关联在至少4个地区具有共同的趋势,表明虽然菌群具有地域差异,但菌群与宿主及环境因子的关联模式却在不同地域之间基本保持一致。其中,我们发现吸烟主要同细菌菌群中Atopobium、Actinomyces、Prevotella显著相关,而大气细颗粒物(PM2.5)浓度主要同真菌菌群中如Cladosporium显著相关(图2)。我们建立污染暴露(吸烟、二手烟、空气污染、生物燃料暴露、职业暴露)、呼吸道菌群(细菌、真菌、宏基因组功能模块、抗生素抗性基因、细菌毒力因子)、呼吸健康指标(肺功能、呼吸道症状评分)的双向中介效应模型,发现呼吸道菌群具在环境污染暴露与呼吸健康指标中具有显著的中介效应。细菌菌群中Peptostreptococcus、Actinomyces、Acinetobacter显著介导吸烟与肺功能的关联。在菌群功能层面,氨基酸分解代谢和次级代谢在吸烟者中显著升高,而氨基酸合成代谢及能量代谢显著降低。Acinetobacter显著贡献了多个功能基因或通路的中介效应,包括苯丙氨酸代谢途径、四环素抗性基因tet32及菌群毒力因子PNAG。同时,真菌显著介导PM2.5与肺功能的关联,其中Penicillium和Cladosporium最为显著。
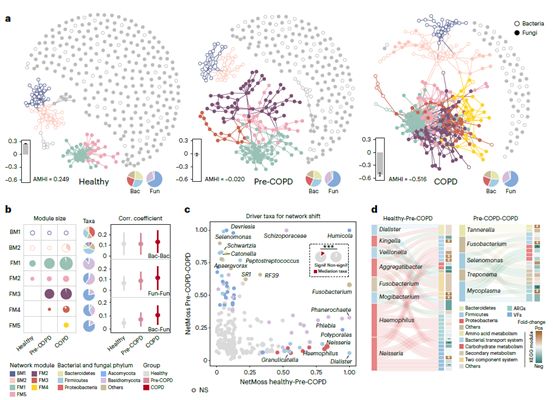
图2. 呼吸道菌群介导环境污染暴露对呼吸健康的影响
(a)呼吸道菌群(多样性、细菌组分、真菌组分、KEGG模块、抗生素抗性基因、毒力因子)与环境暴露因子及、肺功能及呼吸道症状的关联;(b)污染暴露因子与肺功能及呼吸道症状的关联及双向中介效应分析的模式;(c)双向中介效应分析结果概况;(d)具体呼吸道菌群物种及功能的中介效应模式示例图。
职业污染暴露对呼吸道症状的影响与呼吸道菌群相关
我们对呼吸道菌群、环境污染暴露和呼吸健康指数之间建立交互式统计模型,发现呼吸道菌群、职业污染暴露与呼吸道症状评分之间具有显著相互作用。其中,呼吸道细菌菌群第一主成分与职业暴露史具有显著交互作用,共同影响呼吸道症状CAT评分。在细菌分类单元中,Neisseria是唯一具有同职业暴露与呼吸道症状具有显著相互作用的菌属,且其同菌群第一主成分显著相关。据此,我们基于Neisseria将人群分为两个亚组,发现这两组人群中呼吸道症状评分与职业污染暴露之间的关联具有显著差异。相对于Neisseria-low亚组人群,在职业污染暴露影响下,Neisseria-high亚组人群呼吸道症状风险增加2.25倍(图3)。同时,在基于Neisseria所划分的两组人群中,职业污染暴露与呼吸道微生物群落的关联模式也具有显著差异。在Neisseria-high人群中,职业污染暴露与一个独特的呼吸道真菌变化模式显著相关,包括Aspergillus和Penicillium等包含病原真菌的分类单元。同时,11个与细菌粘附和外毒素相关的毒力因子也在Neisseria-high人群中显著同职业暴露相关。这些结果提示,呼吸道菌群中Neisseria富集的人群,在职业暴露污染的影响下,具有导致呼吸道症状的更高风险,且呼吸道真菌菌群的改变在其中发挥了潜在作用。
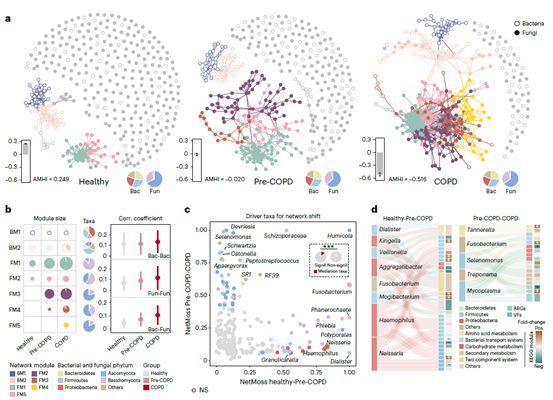
图3. 呼吸道菌群与职业暴露显著互作,共同影响呼吸道症状
(a)呼吸道菌群多样性、环境暴露、肺功能及呼吸道症状的统计交互作用;(b)基于细菌菌群第一主成分与Neisseria的人群分层中,职业暴露与呼吸道症状的关联具有显著差异;(c)Neisseria-high及Neisseria-low人群中职业暴露对呼吸道菌群具有不同的影响;(d)Neisseria-high人群中,职业暴露与真菌菌群中Aspergillus和Penicillium的增加具有独特关联。
呼吸道菌群健康指数可能指示个体污染暴露风险
我们对肠道菌群健康指数的算法进行了修正,以同时纳入呼吸道细菌与真菌的菌群特征,据此测算了个体化的呼吸道菌群健康指数(Airway Microbiome Health Index,AMHI)。我们发现AMHI随着污染暴露、呼吸道症状及呼吸疾病同步发生变化(图4)。其中污染暴露史中的因素种类越多,AMHI下降越显著。同时,AMHI显著介导职业暴露、PM2.5浓度与吸烟对呼吸健康的影响,且同生物燃料暴露、二手烟以及职业污染暴露对呼吸道症状的影响具有显著交互作用。提示该指数可能指示个体受污染暴露所导致的潜在呼吸健康风险。我们将基于我们的数据所测算的AMHI评分应用至全球公共呼吸道微生物组数据集,发现其在不同公共数据的疾病人群相对健康人群具有统一下降趋势,且在部分研究的疾病组与健康组中具有显著差异,提示该评分具有一定的普适性。以上结果表明呼吸道菌群指数可指示污染暴露对呼吸健康的影响。
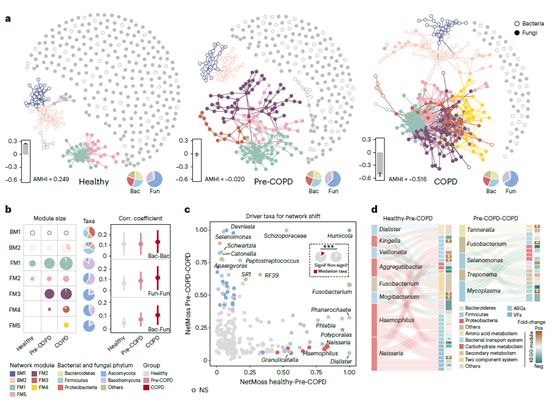
图4. 呼吸道菌群健康指数及其与环境污染暴露的关联
(a)呼吸道菌群健康指数(AMHI)算法;(b)AMHI对呼吸健康的指示功效;(c)AMHI在呼吸疾病与呼吸道症状中的变化;(d)AMHI随着环境暴露因素增加逐渐降低;(e)AMHI、污染暴露与呼吸健康的中介效应分析;(f)AMHI在呼吸道菌群全球公共数据中的应用。
呼吸道细菌-真菌互作可能指示早期慢阻肺发生发展
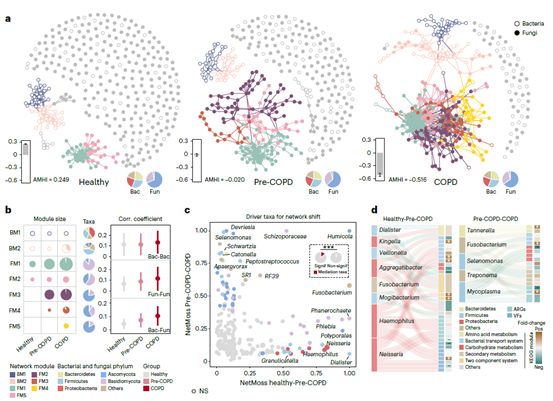
环境污染暴露是早期慢阻肺发生的重要风险因子。在此研究中,190名居民可通过肺功能诊断为慢阻肺(COPD),93.7%处于早中期。我们将未诊断为慢阻肺,但有污染暴露史及显著呼吸道症状的人群定义为慢阻肺风险人群(Pre-COPD)。通过多元网络分析,我们发现呼吸道细菌-真菌的交互作用从健康人群、慢阻肺风险人群、到慢阻肺患者中显著增强(图5),且在COPD中发生了细菌与真菌(包括Aspergillus和Penicillium)互作模块的融合。在Pre-COPD和COPD网络中亦出现了独特的真菌-真菌相互作用模式。环境污染暴露也导致呼吸道细菌-真菌互作的增强,其中吸烟导致的互作网络的变化最为显著。我们通过NetMoss算法鉴定网络变化中的驱动物种,发现变形菌门(如Haemophilus和Neisseria)显著贡献了从健康人群到Pre-COPD人群的网络变化,而拟杆菌门贡献了从Pre-COPD到COPD人群中的网络变化。这些网络变化的细菌驱动者同时显著贡献了从健康人群到慢阻肺患者的菌群功能变化,包括二组分系统、物质转运系统、碳水化合物代谢和次级代谢等。据此我们提出,环境污染暴露可能影响呼吸道菌群跨界互作,其可能进一步导致早期慢阻肺菌群功能失调。
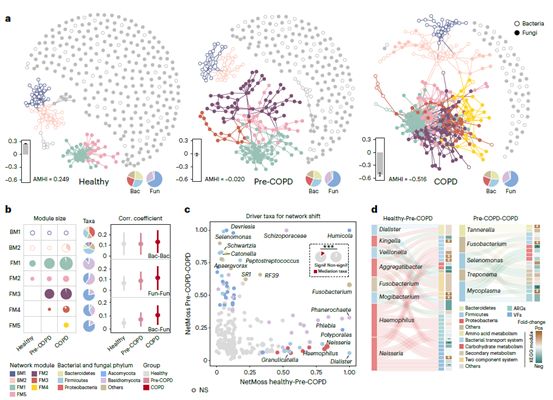
图5. 呼吸道跨界菌群互作网络在早期慢阻肺中的变化
(a)呼吸道细菌-真菌互作网络在健康,Pre-COPD,COPD人群中的发生显著变化;(b)菌群互作网络的模块分析;(c)菌群互作网络变化的驱动物种分析;(d)互作网络变化的细菌驱动者对菌群功能变化的贡献。
讨论
通过大规模人群呼吸道菌群分析,我们揭示了环境污染暴露通过呼吸道菌群影响呼吸健康的可能方式。同肠道菌群类似,地域差异显著影响呼吸道菌群。尽管如此,“环境-菌群-宿主”的关联在不同地域中具有一致性。我们发现呼吸道菌群不仅介导环境暴露与呼吸健康的关联,其可能进一步同环境暴露因子相互作用,来改变它们对呼吸健康的影响。因此,对人群呼吸道菌群的测定有助于对污染暴露的健康影响进行风险分层与精准评估,且对于不同的污染暴露因素需要考虑不同的呼吸道细菌或真菌组成。基于呼吸道细菌与真菌群落结构,我们测算了菌群健康指数及互作网络,这些方法不同于传统基于差异物种丰度的菌群分析,可能为污染暴露对呼吸健康的影响及早期慢阻肺的发生提供新型标志物。
本研究仍具有较多局限性。首先,本研究是观察性、横断面研究。虽然使用了可应用于因果效应推断的中介效应分析,但菌群与环境暴露及呼吸健康的因果关系仍无法直接建立。其次,痰液是口腔及上下呼吸道的内在混合物,因此我们无法评估所得到的菌群物种及分类单元在呼吸道不同结构部位的分布。再次,由于痰液样本量的影响,仅有部分样本能够完成细菌和真菌的同时扩增和测序,且痰液宏基因组中的高宿主比例仍是领域重要挑战。呼吸道病毒组未能获得足够的覆盖度,因此未纳入进一步分析。后续对于呼吸道菌群和环境样本的配对分析可为环境和人体呼吸道之间的菌群交流提供线索。最后,我们的研究结论需要进一步在不同国家、不同人种、不同暴露史的人群中进行验证。
综上,该研究揭示了呼吸道菌群在污染暴露、呼吸道症状与呼吸健康中的关键作用。“环境暴露-呼吸道菌群-健康指标”的交互作用可为环境污染暴露对人体呼吸健康的影响提供潜在的菌群风险因子。呼吸道菌群可能影响环境污染暴露的个体健康效应,为基于呼吸道菌群的环境污染暴露风险分层,及靶向呼吸道菌群的风险预防提供科学依据。
作者简介
华南师范大学王璋、广东省疾控中心林立丰、郑雪燕、孙九峰、广州医科大学附属第一医院—广州呼吸健康研究院关伟杰为本文的共同通讯作者。广东省疾控中心林立丰、华南师范大学易歆竹、厦门大学附属第一医院刘海月、广东省疾控中心孟瑞琳为本文的共同第一作者。本研究得到了国家重点研发计划、国家自然科学基金、广东省自然科学基金、广州市科技计划、广东省钟南山医学基金会、广州医科大学科研提升计划等项目的资助。
相关知识
代谢健康肥胖:从流行病学、机制到临床意义
瘦型非酒精性脂肪性肝病的研究进展
16:8轻断食,减肥又健康,但要选对时间!最新研究:“过午不食”才是关键,还能改善血糖
特别关注:瘦型非酒精性脂肪性肝病
肺康复治疗
临床问题|2020瘦型
重磅!中国院士团队:这类患者血压降到 120mmHg 更好,NEJM:标准能改了?
肠道菌群及其代谢产物与妊娠期糖尿病相关性的研究进展
孕期睡眠障碍的流行病学研究进展
50% 以上成人存在超重或肥胖!不只影响审美,还有这些危害
网址: Nat Med https://www.trfsz.com/newsview48100.html
推荐资讯
- 1发朋友圈对老公彻底失望的心情 12775
- 2BMI体重指数计算公式是什么 11235
- 3补肾吃什么 补肾最佳食物推荐 11199
- 4性生活姿势有哪些 盘点夫妻性 10428
- 5BMI正常值范围一般是多少? 10137
- 6在线基础代谢率(BMR)计算 9652
- 7一边做饭一边躁狂怎么办 9138
- 8从出汗看健康 出汗透露你的健 9063
- 9早上怎么喝水最健康? 8613
- 10五大原因危害女性健康 如何保 7828






