健康监测传感器的研究进展
来源: 时间:2024年11月25日 08:07
从身体中检测其他物理和化学信息将使基本健康的精确监测和各种疾病的早期诊断成为可能。下面简单介绍下皮肤附着化学和电生理传感器的最新进展。化学传感器生物液体通常含有电解质、代谢物和激素。因此,检测和分析这些生物标志物的化学传感器将在分子水平上提供重要的生理信息,从而使疾病的早期诊断和预防成为可能,例如,重金属的短缺和过剩都会对人体产生有害影响。因此,不断监测重金属浓度可以采取适当的行动。在这方面,用于医疗目的的皮肤附着化学传感器受到高度追捧。在过去几年,许多研究工作都集中在化学传感器上,这些传感器通常安装在可弯曲的衬底上,以确保佩戴者的舒适度。
化学传感器的工作原理
化学传感器主要由电化学器件、化学电阻和晶体管组成。一旦暴露在目标化学物质中,这些装置通常显示出电位、电流或电阻的变化。电化学传感器(包括参考电极、工作电极和辅助电极)对目标分析物的暴露会导致电位(带电分析物)或电流(氧化还原活性分析物)的变化。例如,电位传感器通常使用离子选择电极选择性地响应目标分析物,而在安培传感器中,电极固定化酶催化目标材料的氧化还原反应。化学电阻由两个电极之间的传感元件组成;传感元件的电阻在接触目标分析物时发生变化。最后,基于晶体管的化学传感器具有一个半导体层、一个介电层和三个(源极、漏极和栅极)电极。换句话说,晶体管可以被看作是加入了介电层和栅电极的化学电阻,以允许信号放大和高灵敏度。在实际应用中使用化学传感器需要考虑许多因素。例如,人体中的生物体液含有低浓度的化学物质;因此,实际应用的化学传感器应具有高选择性、低检测限、高灵敏度(精确测定分析物浓度)和高重复性。体液的获取
血液是临床应用最广泛的生物体液;然而,侵入性针刺提取血液限制了它们的实时和长期使用。因此,皮肤可附着化学传感器需要生物液体的微创或非侵入性获取。例如眼泪、唾液、尿液、汗液和间质液。在这些生物体液中,对眼泪、唾液和尿液样本的分析给使用者带来了不便。因此,汗水和ISF传感器更适合长期使用和舒适。出汗是通过剧烈运动或受热产生的。然而,汗液的化学成分动态地反映了人体的生理变化,因此依赖于刺激机制。换句话说,运动或高温所产生的汗的成分可能不能代表正常的健康状态。因此,健康监测需要使用局部和随需应变的排汗技术,如离子导入,这一过程利用一种称为匹罗卡品的致汗化合物刺激局部排汗(图1a)。具体来说,一股温和的电流会导致皮罗卡品流入皮肤,刺激汗腺,从而导致汗液的释放。超过100 nL min - 1 cm - 2的分泌物可在不引起任何不适的情况下获得,这种无创安全排汗技术已获得FDA批准。同样,ISF也可以通过反向离子透入获得(图1a)。与直接离子透入不同的是,反向离子透入不需要使用药物,它是基于某些化学物质(如ISF中的离子和葡萄糖)在轻微电流作用于表皮后向皮肤表面的迁移。单一设备还可以通过结合直接和反向离子导入同时提取汗液和ISF,实现多路化学传感。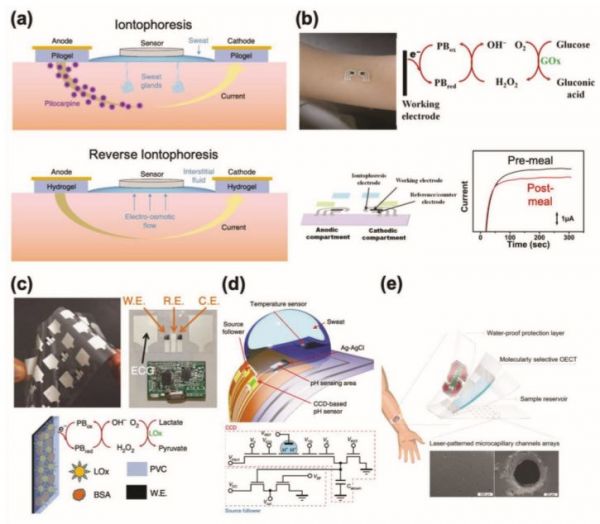
图1
汗液传感器
在过去的几年中,可穿戴式汗液传感器领域取得了显著的进展,例如,用于分析葡萄糖、乳酸盐、乙醇、pH和电解质的多种汗液传感器的开发。这些可穿戴汗液传感器大多由电化学电极组成。具体来说,安培法常用于乙醇和代谢物的酶学检测,而带电物质的检测多采用电位法。如前所述,安培传感器通常利用生物分子的氧化还原反应。在这种装置中,诸如乳酸氧化酶、葡萄糖氧化酶和酒精氧化酶等酶被固定在电极上,以便对目标分析物进行选择性的氧化/还原。由于所测电流随分析物浓度的增加而增大,因此可以由分析物浓度推算出后一个参数。如图1c开发了一种皮肤穿戴式可穿戴传感系统,它可以检测乳酸盐和心电信号。具体来说,乳酸传感器利用了一个与乳酸氧化酶功能化的工作电极,其中电流的增加与汗液中的乳酸浓度相关。离子选择电极常用于电位传感器,如以前开发的用于检测汗液中带电物质(如铵离子、钾离子和钠离子以及质子)的传感器。离子选择电极的电势很大程度上取决于目标分析物的浓度,因此可以从工作电极和参考电极之间的电势差来推断分析物的浓度。尤其是离子选择电极被使用,在那里离子浓度的增加导致一个潜在的变化。这种电位分析本质上遵循Nernst方程,即在美国,电解液传感器的灵敏度被限制在每一数量级的浓度差异59 mV。图1d使用了一种充电的设备来开发一种pH传感器,这种传感器的灵敏度超过了这个极限,通过电子电荷转移周期的积累,使其灵敏度达到了240 mV pH−1。更重要的是,这一策略有可能应用于使用离子敏感膜检测其他电解质。附在人手臂上的pH感知系统成功地实时监测pH值和温度。生物体液中的激素也可以用化学传感器来表征。然而,可靠的激素传感器的实现受到它们在生物液体中的极低浓度的阻碍。例如,尽管皮质醇(一种指示压力水平的激素)作为一种生物标志物很重要,但在汗液中检测到它的研究却很少。图1e是一种基于有机电化学晶体管(OECTs)的皮质醇传感器,该传感器包含一个分子印迹层,可以选择性地与皮质醇结合。在这个传感器中,皮质醇分子和印迹层之间的结合阻碍了离子的运动,最终阻止了活性层的掺杂,这使得皮质醇浓度可以从电流的变化中推断出来。这种基于嗅鞘细胞的皮质醇传感器被应用于人的前臂,用于实时监测汗液中的皮质醇。运动后,皮质醇传感器的电流变化显著,而控制装置的反应可以忽略不计。此外,用于多路复用的完全集成的化学传感器是非常受欢迎的。虽然单分析生物传感器可以提供一些关于健康的信息,但对这些信息的解释有时可能会产生误导,因为多种因素可能导致相同的结果。相反,当多个传感器集成到一个平台上时,生理事件的实际原因可以清楚地识别出来。研究人员制作了完全集成的可穿戴传感器,用于汗液的现场分析(图2a)。该传感器平台同时表征葡萄糖、乳酸盐、钠离子和钾离子浓度,同时利用温度信息进行校准。更重要的是,不需要外部分析,所有必要的信息都可以无线传输到便携设备和云服务器上。图2a中将加热器、温度、湿度、葡萄糖和pH传感器集成到一个皮肤可连接设备中。一旦汗液分泌达到一个临界湿度值,葡萄糖传感器就开始与温度和pH传感器同时工作,从而纠正了葡萄糖读数。这个集成的装置还包含了微针,可以在暴露在高温下释放治疗糖尿病的药物。葡萄糖传感器测得的高浓度葡萄糖激活加热器,从而触发药物释放。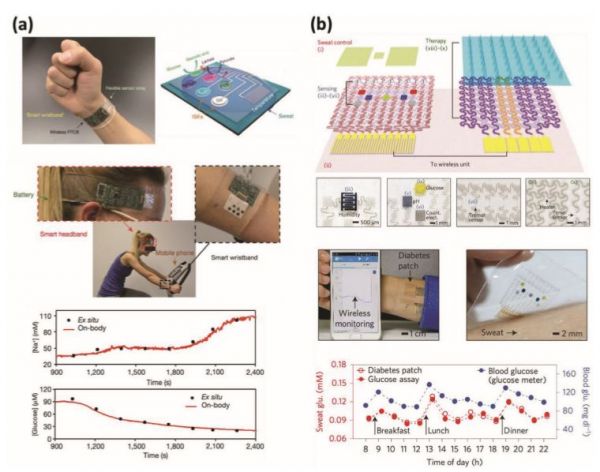
图2
ISF传感器
2001年,FDA批准了第一个商业化的非侵入性葡萄糖传感器GlucoWatch。这些腕带型传感器利用反向离子导入法提取ISF并分析其血糖水平,这可能与血糖水平有关。重要的是,GlucoWatch进行了周期性的血糖浓度测量,这是糖尿病患者所希望的。然而,很多使用GlucoWatch的用户报告称,他们感到不适和皮肤刺激,这些传感器的生产随后被淘汰。最近,有人制作了纹身样葡萄糖传感器(图1b),显示了食物摄入后葡萄糖水平显著升高。皮肤样的无创葡萄糖传感器也被开发出来,允许ISF中的葡萄糖浓度与血液之间的精确关联。最后,将ISF传感器与汗液传感器集成在一起进行多重分析,例如同时测量汗液中乙醇和ISF中葡萄糖的含量。这种用于双表皮液分析的皮肤可附着传感器系统可以进一步开发,以同时监测各种生物标志物。用于检测生物电位信号的电生理传感器鉴于器官、组织和神经活动与电势有关,监测电生理(EP)信号有助于发现异常生命体征。特别是心脏(心电图:ECG)、肌肉组织(肌电图:EMG)、大脑(脑电图:EEG)等相关疾病可通过EP监测系统进行诊断。一般情况下,EP传感器由三种电极(记录电极、参考电极和接地电极)与皮肤共形接触(图3a)。接地电极被连接在一个零电位区,因为它们定义了一个感觉电路的基线,而记录和参考电极分别被放置在目标的身体部分和四肢。例如,一个ECG传感器需要10个电极,其中6个连接到靠近心脏的胸腔(目标身体部位),而其余4个电极则放置在四肢(胳膊和腿)上。这10个电极读取12个不同电极组合记录的独特电信号,使医生能够诊断不同解剖区域的异常心脏活动。
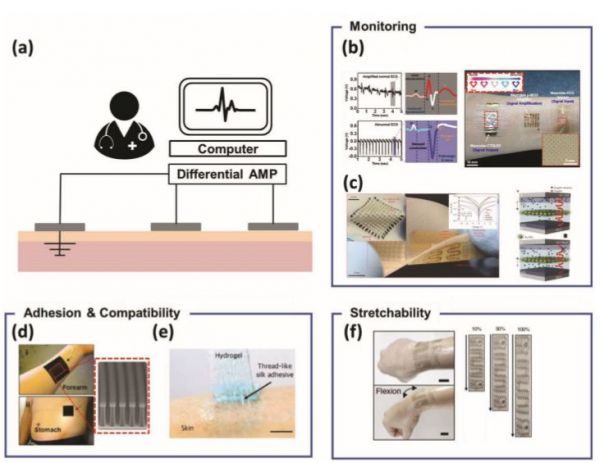
图3
传统的EP传感系统的特点是用胶带、夹子或粘垫将大块电极贴在身体的目标区域。此外,电极使用导电医用凝胶与皮肤保持接触。虽然该平台可以实现准确的电读,但由于大型、刚性、重电极的限制,使用该平台对患者不方便。为了克服这些限制,Rogers和他的同事引入了一种新的概念,一种柔软的、超薄的、轻量级的生物兼容的表皮电子系统(EES)。这种电子设备是通过将丝状蛇形金属连接到柔软的弹性体上,从而调整系统的机械性能,使之与人类皮肤的力学性能相匹配。上述研究人员利用该系统成功地记录了心电图和肌电图,并演示了该系统与应变传感器、无线电源和led等其他电子元件的集成。由于EP信号分析的复杂性,通常由医院的医生监测EP信号。图3b为一种基于有机物的心电监测系统,当检测到异常心电信号时,该系统会改变颜色,可使EP信号监测适合家庭监护。在这个系统中,正常情况下会发出红光,而发出蓝光则是心脏异常活动的警报。在这两种情况下,发射都是通过CNT晶体管放大器和CTOLEDs(颜色可调的有机发光二极管)显示设备实现的。上述EP监测系统只能与外部计算机连接使用。图3c是一种带有存储器的多功能设备,这样就可以不需要外部计算机就可以测量和存储信号。研究人员记录了记忆细胞中的肌肉活动,并监测震颤频率以检测癫痫或帕金森氏症。该器件采用了TiO2-Au NP复合电阻RAM,实现了低功耗运行。而且他们提出了一种便携式EP监测系统的概念验证。电极与皮肤的强附着力,同时确保不使用湿凝胶的电接触也很重要,因为它是一个便携式的现场诊断系统。科研人员开发了一种基于碳纳米复合材料的电极,这种电极具有壁虎脚的表面结构,以其优异的附着力而闻名(图3d)。该电极能够与皮肤产生强烈的电接触和物理接触,允许在活动过程中测量心电图而不需要电极脱落。利用电极材料的化学性质,如钙改性的生物相容性丝素蛋白,也可以制备出强粘附电极(图3e)。在这种情况下,插入Ca2+离子增强了物理联锁在电极-皮肤界面,允许运动下的心电图测量。即使传感装置可以安全地附着在皮肤上,也不应该产生皮肤刺激等副作用。在这方面,有人引入了一个开放的Au纳米网络,它不会干扰皮肤的空气流通,因此有望成为长期EP信号记录的合适接口材料。可拉伸性也是电极的一个重要特征,因为它能使电极与身体形状不规则的区域产生舒适的接触,并且在日常活动中不会防止皮肤在反复拉伸下发生断裂。银钨,可以作为可拉伸电极,提供了许多优势,如优良的导电性和易于加工。但银的生物相容性差、抗氧化性差,仍是其应用的一大难题。在这方面,有人报告了一种基于Ag NWs的镀金层可拉伸电子设备,它结合了Au(生物相容性和抗氧化性)和Ag NWs(优异的导电性和可拉伸性(最大840%))的优点(图3f)。尽管EP信号记录设备不断发展,但由于其独特的性能,在皮肤可接触电子领域的实际应用还远远不够。如,空间限制,因为它们需要与外部计算机连接;长期的化学不稳定性和生物相容性;在日常生活活动中对皮肤电接触和物理接触的低鲁棒性。因此,未来的工作应该集中在具有无线通信能力、更好的化学稳定性、表皮相容性和对皮肤的强附着力的EP传感系统的设计上。参考文献:Jun Chang Yang, Jaewan Mun, Se Young Kwon,Seongjun Park, Zhenan Bao, and Steve Park. Electronic Skin: Recent Progress andFuture Prospects for Skin-Attachable Devices for Health Monitoring, Robotics,and Prosthetics. Adv. Mater. 2019, 1904765.相关知识
柔软灵活的无线传感器可监测婴儿和产妇健康
研究进展
胎动监测器
桥梁健康监测数据分析研究综述.pdf
全生命周期健康监测诊断系统研究
用于健康与健身应用的传感器技术
智能复合材料在健身器材中的健康监测
生态系统健康研究进展
慢性病的健康管理研究进展
标签:“健康监测”
网址: 健康监测传感器的研究进展 https://www.trfsz.com/newsview76503.html
推荐资讯
- 1发朋友圈对老公彻底失望的心情 12775
- 2BMI体重指数计算公式是什么 11235
- 3补肾吃什么 补肾最佳食物推荐 11199
- 4性生活姿势有哪些 盘点夫妻性 10428
- 5BMI正常值范围一般是多少? 10137
- 6在线基础代谢率(BMR)计算 9652
- 7一边做饭一边躁狂怎么办 9138
- 8从出汗看健康 出汗透露你的健 9063
- 9早上怎么喝水最健康? 8613
- 10五大原因危害女性健康 如何保 7828
资讯热点排名
资讯热点






