Cell Metabolism
肥胖是一种异质性、复杂性的代谢性疾病,全球约有39%成年人出现超重,13%人群发生肥胖,肥胖的高流行率原因可部分归因于高热量食物摄入和久坐不动的生活方式。体重过重会使糖尿病和心血管等疾病的风险显著增加。当前通过体重指数(BMI)粗略测量并不能解释肥胖的表型特征,需要一种更精确且简便的表型分类方法对肥胖患者进行分类以便于临床管理和药物干预。已有研究报道肥胖患者具有支链和芳香族氨基酸、甘油和甘油磷酸胆碱水平增加的代谢表型。Cirulli团队采用非靶向代谢组学和全基因组测序对2,396例具有BMI、拟人数据、全身DEXA扫描及代谢组的纵向测量结果与基线遗传风险相结合的个体血浆样本进行检测,深入研究肥胖的代谢和遗传特征,相关研究成果发表于国际知名期刊《Cell Metabolism》。
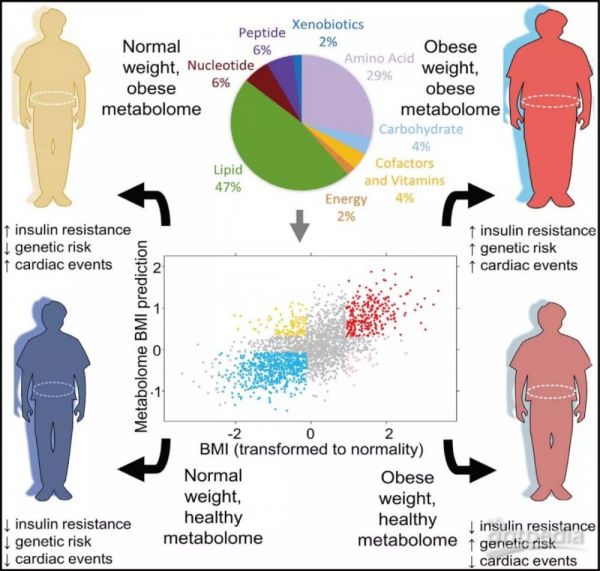
与BMI相关的肥胖代谢物
通过对不同人群3个时间点(时间跨度8-18年)的血浆样本进行检测,共鉴定1007个代谢物,其中307个代谢物至少在一个人群和一个时间点与BMI相关,进一步分析筛选出49种代谢物与BMI的关联性最强(图1,表1),主要是脂质(n = 23,占两个群组中测定的所有脂质的7.5%),氨基酸(n = 14,占所有氨基酸的9.3%),核苷酸(n = 3,所有核苷酸的12.0%),肽(n = 3,所有肽的12%)和其他类别(n = 6),其中最显著相关的代谢物是尿酸。这些代谢物水平和BMI呈线性相关(图1C),其中35种代谢物随着BMI的增加而增加,如葡萄糖和甘露糖,支链和芳香族氨基酸、核酸代谢相关的代谢物如尿酸的增加最快;部分代谢物随BMI升高而降低(n = 14)如磷脂和溶血脂、氨基酸天冬酰胺、N-乙酰甘氨酸、肉桂酰甘氨酸。负相关脂质反映HDL(高密度脂蛋白)水平,而正相关脂质更能代表甘油三酯水平(表1和S1),尤其注意到BMI和皮质酮(类固醇激素皮质醇的代谢产物)的相关性。通过主成分分析检验了这些代谢物分布的总体组成,第一主成分解释了49种代谢物水平总变异的20%。对49种正常体重、超重或肥胖的代谢物分别进行了检测,发现它们的作用方向与整个小组的结果基本一致(表S1)。
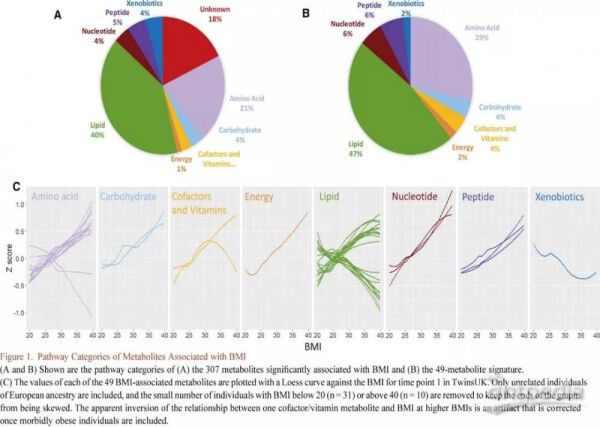
肥胖代谢组模型
基于BMI相关的49种代谢物采用岭回归建立了一个BMI预测模型(定义为mBMI)(图2),将其应用于TwinsUK和Health Nucleus队列分析,对随机一半的人群进行建模及十折交叉验证,作为测试集的另一半数据中发现该模型可以解释BMI变异的39.1%(图2A)。在预测参与者是肥胖(BMI ≥30)或正常体重(BMI 18.5-25)时,该模型的曲线下面积(AUC)为0.922,特异性为89.1%,敏感性为80.2%。与49种代谢物建模相比,使用非靶向代谢组建模(在两个群组中测量n = 650)提高了模型的准确性(可解释方差47%-49%),常规临床指标包括年龄、性别、HDL、LDL、总胆固醇和总甘油三酯建模回归分析解释了BMI变异的31%,而使用年龄、性别和49种代谢物的模型解释了43%的变异。
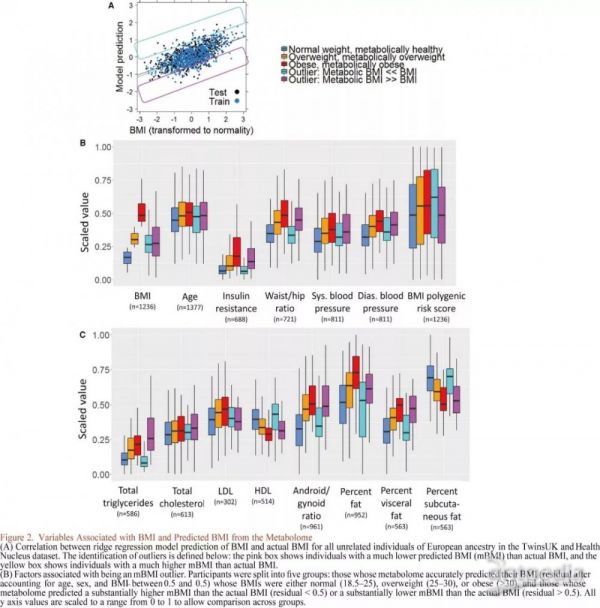
BMI代谢异常值的鉴定和表征
基于已经建立的代谢组预测BMI的模型(mBMI),将参与者分成五组(图2A),三组预测被定性为正常值,包括正常BMI(18.5-25)、超重(25-30)或肥胖(> 30),两组被定性为异常值:代谢组预测mBMI << 实际BMI(具有正常体重健康个体相似的代谢组)或mBMI >> 实际BMI的个体(具有与肥胖个体相似的代谢组)。两个异常组具有相同的体重和年龄分布(图2B),但其表型差异显著(图2B和2C),如具有肥胖代谢表型的正常BMI和具有健康代谢表型的肥胖BMI通常证实了这些效应(图3和S2)。本研究结果表明,代谢组是用于代谢扰动背景下肥胖症临床研究的有效工具,可用于识别代谢“健康”肥胖及正常BMI个体但代谢健康状况不佳的人群,而非单独依靠BMI表征。为了分析两组异常值人群代谢变化,通过采用与BMI相关的49种代谢物进行分析,虽然两组BMI分布相同,但天冬酰胺和肾上腺皮质酮除外的其他代谢物水平上存在显著统计学差异(图S3)。皮质酮是皮质醇的代谢产物,据报道皮质醇与肥胖有关,而皮质醇全天都在变化,并非所有的参与者都同时检测,因此该因素可能影响实验结果。此外,还研究了每种BMI相关代谢物与胰岛素抵抗之间的关联,对515名无关的欧洲血统参与者进行定量胰岛素抵抗测量, BMI控制之后,发现49种BMI相关代谢物中的12种(酪氨酸、丙氨酸、犬尿酸、γ-谷氨酰酪氨酸、1-油酰基-3-亚油酰基-甘油(18:1/18:2)、六种磷脂和预期的葡萄糖)与胰岛素抵抗呈显著正相关。
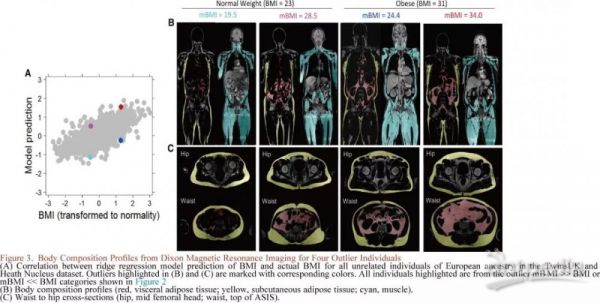
mBMI在肥胖、心血管疾病和双胞胎间相关性的应用
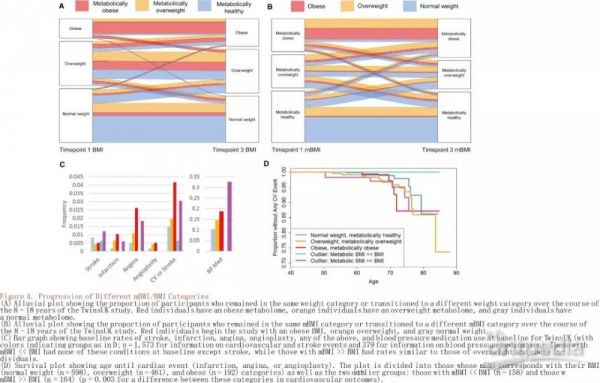
mBMI异常组是否更有可能随着时间的推移演变成肥胖?作者对TwinsUK队列的1458名个体分三个时间点进行体重测量,结果mBMI高于BMI的人群(8-18岁)体重增加且转为肥胖表型(BMI> 30)的可能性较大。
对TwinsUK 队列1,573名个体(基线前有32例心血管患者)进行研究,发现mBMI << BMI没有既往心血管病史,而mBMI >> BMI具有一定比例的心血管病史,类似于超重和肥胖个体(图4C)。从379名基线人群使用血压药物史中发现mBMI >> BMI血压药物使用率显著高于mBMI << BMI人群(图4C)。TwinsUK纵向随访13年(中位值)的研究记录了53例受试者发生心血管时间,本研究结果显示该模型有80%的能力来确定不同mBMI/BMI组的心血管事件,健康代谢组个体(正常BMI,超重或肥胖)的发生率为2.6%,肥胖代谢特征的个体mBMI为3.4%(正常/超重BMI)和4.4%(在肥胖个体中)。对参与者进行生存分析,发现具有更健康代谢表型的人群可以更少/更晚发生心血管事件(图4D)。
鉴于双胞胎研究在分析性状遗传性方面的重要作用,作者重新评估了350对双胞胎的BMI模型预测和肥胖状态,该模型的高特异性和敏感性提示基于代谢物组的肥胖预测反映了个体的实际肥胖状态,基于代谢物肥胖预测之间的相关性在同卵双胞胎之间显著高于双卵双胞胎。同时确定了三组双胞胎,其中双胞胎通过代谢组预测为正常体重,但两者都是肥胖,八组双胞胎结果相反,这些异常值被认为代表健康型肥胖和正常体重代谢不健康的个体。
遗传分析
已知的肥胖遗传学
根据肥胖和BMI GWAS文献中已知关联计算了BMI的多基因风险评分(polygenic risk score,PG)。作者研究了最高PG的独特个体是否会对代谢组、拟人化、胰岛素抵抗和DEXA测量产生显著扰动(图5),结果显示较高的PG与男女体型比例、腰/臀比、甘油三酯相关联,与mBMI之间没有统计学关联。
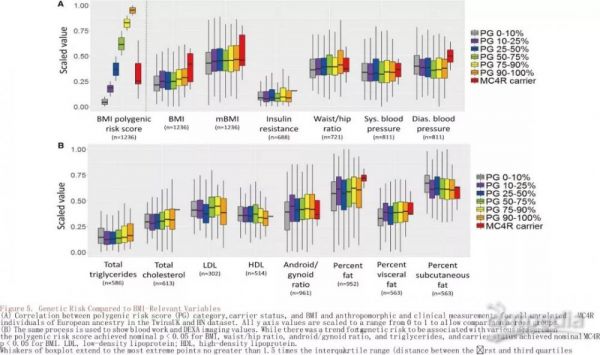
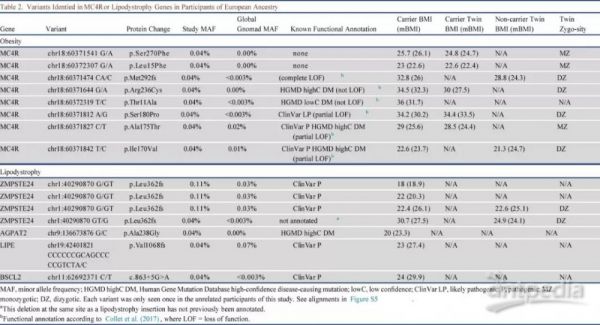
对肥胖症中罕见变异体黑皮质素4受体(MC4R)突变,本研究鉴定携带稀有等位基因频率(MAF <0.01%)的编码变体,共确定了8个载体(表2),其中六个在临床数据库HGMD 或 ClinVar中已注释为具有引起肥胖的作用(表2)。MC4R携带者的BMI显著高于非携带者,对于更高的舒张压、胰岛素抵抗和体脂百分比没有显著的变化趋势(图5)。在携带相同MC4R变体的五组双胞胎中,三组为超重或肥胖,另两组在没有MC4R基因变异的两例携带者中,他们的BMI低于其双胞胎。作者观察到MC4R变异携带者在多基因风险评分低的肥胖个体中数量较多,在37名肥胖且PG最低的参与者中,5.4%是MC4R变异携带者,而正常体重的携带者仅为0.4%。此外,在研究人群中搜索与孟德尔脂肪营养不良综合征相关的罕见变异,在四个基因中鉴定了六个具有罕见杂合变体的个体:ZMPSTE24,AGPAT2,LIPE和BSCL2(表2),有LIPE或BSCL2变异的个体体重正常,但属于mBMI >> BMI异常组。
代谢健康肥胖与代谢组差异的遗传学
mBMI << BMI的个体在BMI上的PG高于其他组,反之mBMI >> BMI个体具有低的PG(图2B),可见BMI的PG可能会捕捉到一个拟人化的表型(体型较大的个体)而不是与肥胖作为疾病特征的独特关联。接下来作者研究了具有不同遗传背景的肥胖个体是否具有与其他肥胖个体不同的代谢组。首先搜索了可以区分具有不同BMI的PG或MC4R变异携带者的代谢物,线性回归显示,在整个人群中或仅在肥胖个体中,任何单一代谢物与多基因风险或MC4R携带者状态之间没有显著关联。这一结果意味着代谢物不太可能是解释肥胖潜在遗传学的中间表型。为了检查更多PG之外的信号,对用于计算PG的97种变体进行了单独分析,没有发现任何证据表明这些已知的GWAS变异与代谢产物的联系比与BMI本身的联系更紧密,因为大多数个体GWAS变异的影响很小。综上,虽然代谢物水平有很强的遗传成分,但大多数发生在肥胖状态的代谢紊乱是对肥胖的反应,而不是遗传机制。
小结
本研究检测了约1000个代谢物,其中307个与BMI相关,49个代谢物被选为建立预测BMI(mBMI)模型以研究BMI、肥胖、代谢疾病和基因之间的关系,结果显示与BMI最显著相关的单一代谢物是尿酸,同时发现脂质与BMI显著相关。本研究方法可用于构建胰岛素抵抗、脂肪分布或其他临床类似模型,并且mBMI代谢组特征可作为MC4R突变患者的生物标志物。代谢健康的肥胖人群具有高BMI多基因风险评分, 携带MC4R变异体的肥胖人群有低的多基因风险评分。本文将研究重点主要集中在肥胖测量指标BMI上,其独特丰富的代谢组学和表型数据为肥胖相关的健康调查奠定了基础,但仍需要建立如糖尿病或内脏脂肪等其他代谢特征模型,同时设计实验验证在mBMI / BMI类别和纵向心血管结果之间观察到的关联。这种结合多种代谢物来评价肥胖和健康状况的方法仍处于研究阶段,要想通过代谢物来对疾病进行预测,还需要更长时间的跟踪调查和临床试验的验证。
参考文献
E.T Cirulli, L.N Guo, A. Telenti, et al(2019). Profound perturbation of the metabolome in obesity is associated with health risk . Cell Metab. 29, 1–13.

长按关注
解锁更多更精彩的「代谢组学」相关资讯!
微信公众号:麦特绘谱
Tel:400-867-2686
Web: www.metaboprofile.com
相关知识
Cell封面:中国科学家发现减肥新途径,通过激活白色脂肪棕色化实现抗肥胖
Cell子刊:GDF15与瘦素协同作用,进一步加强减肥效果
Cell子刊:代谢不健康的“瘦子”,比健康的“胖子”更危险
GLP研究成果闪耀《Cell》,哈佛减肥科技突破,都市女性的减重福音
绿瘦新知 Cell子刊揭示「天生瘦子」的奥秘竟是它
快速減肥怎麼做?14個快速減肥方法大公開!保證快速瘦身減脂
关注婴儿早期糖代谢,预防孕期空气污染相关的神经发育迟缓
全球首例!Cell 最新:中国团队成功治疗 1 型糖尿病
节食减肥后体重反弹真不赖你!Cell 子刊:科学家发现驱动节食后体重恢复的神经回路,会让你更饿!
Cell子刊:膳食纤维虽好,摄入也要因人而异
网址: Cell Metabolism https://www.trfsz.com/newsview77906.html
推荐资讯
- 1发朋友圈对老公彻底失望的心情 12775
- 2BMI体重指数计算公式是什么 11235
- 3补肾吃什么 补肾最佳食物推荐 11199
- 4性生活姿势有哪些 盘点夫妻性 10428
- 5BMI正常值范围一般是多少? 10137
- 6在线基础代谢率(BMR)计算 9652
- 7一边做饭一边躁狂怎么办 9138
- 8从出汗看健康 出汗透露你的健 9063
- 9早上怎么喝水最健康? 8613
- 10五大原因危害女性健康 如何保 7828






